
元素R有如下反应:RO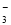 +5R-+6H+===3R2+3H2O,下列说法正确的是( )
+5R-+6H+===3R2+3H2O,下列说法正确的是( )
A.元素R位于周期表中第ⅤA族
B.RO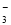 中的R只能被还原
中的R只能被还原
C.每反应消耗1 mol RO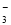 ,转移电子的物质的量为5 mol
,转移电子的物质的量为5 mol
D.R2在常温常压下一定是气体
科目:高中化学 来源:2013-2014山东省淄博市高一下学期期末考试化学试卷(解析版) 题型:填空题
(9分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列
问题:
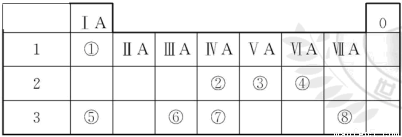
(1)④、⑤、⑥的原子半径由大到小的顺序是____________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是____________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:_____________________________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)_______________________________________。
a.MnO2b.FeCl3c.Na2SO3d.KMnO4
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高二化学试卷(解析版) 题型:选择题
某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1∶2,下列说法正确的是 ( )
A.分子中C、H、O个数之比为1∶2∶3 B.分子中C、H个数之比为1∶4
C.分子中一定含有氧原子 D.此有机物的最简式为CH4
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高一化学试卷(解析版) 题型:推断题
(10分)下列框图中,已知A、E、F、H是单质,其中只有A是固体,其它都是气体,且H是呈黄绿色;B是最常见液体,G的焰色反应呈黄色,L是白色沉淀,M是红褐色沉淀。部分反应的某些产物未标出。
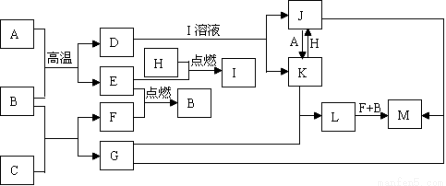
(1)写出H的化学式: 、C的电子式: 。
(2)写出D与I溶液发生反应的离子方程式: 。
(3)写出L→M的化学方程式: 。
(4)检验J中的阳离子时,不宜选用下列试剂中的 (填选项字母)。
A.Fe粉 B.NaOH溶液 C.KSCN溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高一化学试卷(解析版) 题型:选择题
关于反应中的先后顺序,下列评价正确的是( )
A.向浓度都为0.1mol·L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应
B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应
C.向浓度都为0.1mol·L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应
D.向0.1mol·L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市3月质量检测高一化学试卷(解析版) 题型:选择题
氯元素的相对原子质量为35.5,氯只有35Cl和37Cl两种稳定同位素,在氯气中35Cl和37Cl的原子个数比为3∶1,则相对分子质量为70,72,74的氯气分子数之比可能是( )
A.5∶3∶2 B.5∶2∶2 C.5∶2∶1 D.9∶3∶1
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高二年级第二学期阶段考试化学试卷(解析版) 题型:实验题
(12分)氯化钾样品中含有少碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将过滤液按下图所示步骤进行操作。
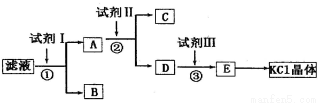
回答下列问题:
(1)起始时滤液的pH_____7(填“大于”“小于”或“等于”),其原因是__________________(用离子方程式表示)。
(2)试剂I的化学式为______,①中发生反应的离子方程式为_____________________。
(3)试剂II的化学式为_____,②中加入试剂II的目的是_________________________。
(4)试剂III的名称是_____,③中发生反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高二年级第二学期阶段考试化学试卷(解析版) 题型:选择题
下列事实不能用勒沙特列原理解释的是( )
A.氨水应密闭保存,放置低温处
B.在FeC12溶液中加入铁粉防止氧化变质
C.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
D.实验室可用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省泰安市高三第二轮复习质量检测理综化学试卷(解析版) 题型:填空题
(12分)【化学——物质结构与性质】
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 ;
②尿素(H2NCONH2)分子中C原子的杂化方式是 ;
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。
Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)下列说法正确的是 (填字母序号)。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl的熔点比CaO熔点低
D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
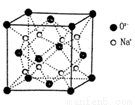
(3)O和Na的一种只含有离子键的化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为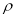 g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含
g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含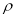 、NA的计算式表示)
、NA的计算式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com