
| A. |  图可表示体积均为V0L、pH均为11的氨水与NaOH溶液分别用水稀释至VL情况,则b曲线为氨水 | |
| B. |  图可表示水溶液中H+与OH-的浓度变化曲线,则升高温度可实现a→b | |
| C. | 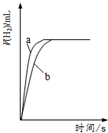 图可表示体积均为100mL、pH均为3的盐酸与醋酸,分别与0.003gZn反应,则a表示盐酸 | |
| D. | 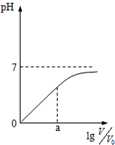 图可表示体积为V0L1 mol•L-1盐酸用水稀释至VL情况,则0~a范围内:pH=lg$\frac{V}{{V}_{0}}$ |
分析 A.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释两种溶液时,促进一水合氨电离,利用两溶液在稀释时强碱的变化程度大来分析解答;
B.升高温度促进水的电离,溶液中氢离子浓度和氢氧根离子的浓度均增大;
C.n(Zn)=$\frac{0.003g}{65g/mol}$=0.00005mol,根据Zn~2H+得,锌完全反应需要n(H+)=0.00005mol×2=0.0001mol,pH=3、100mL盐酸中n(HCl)=0.001mol/L×0.1L=0.0001mol,所以盐酸恰好反应,pH相等的醋酸和盐酸,醋酸浓度大于盐酸,所以pH=3的100mL醋酸中醋酸的物质的量大于盐酸;
D.1 mol•L-1盐酸的pH=0,溶液稀释10n,pH增大n个单位.
解答 解A.一水合氨是弱电解质,氢氧化钠是强电解质,加水稀释溶液促进弱电解质电离,导致稀释溶液氢氧化钠溶液中氢氧根离子浓度变化较大,氨水中氢氧根离子浓度变化较小,pH变化较小,则a是氨水溶液,故A错误;
B.升高温度促进水的电离,溶液中氢离子浓度和氢氧根离子的浓度均增大,a→b的过程中氢氧根离子浓度增大,氢离子浓度减小,所以升高温度不能实现a→b,故B错误;
C.n(Zn)=$\frac{0.003g}{65g/mol}$=0.00005mol,根据Zn~2H+得,锌完全反应需要n(H+)=0.00005mol×2=0.0001mol,pH=3、100mL盐酸中n(HCl)=0.001mol/L×0.1L=0.0001mol,所以盐酸恰好反应,pH相等的醋酸和盐酸,醋酸浓度大于盐酸,所以pH=3的100mL醋酸中醋酸的物质的量大于盐酸,则反应过程中醋酸溶液中氢离子浓度大于盐酸中氢离子浓度,所以醋酸与锌反应的速率快,即a表示醋酸,故C错误;
D.1 mol•L-1盐酸的pH=0,溶液稀释10n,pH增大n个单位,所以体积为V0L1 mol•L-1盐酸用水稀释至VL情况,则0~a范围内:pH=lg$\frac{V}{{V}_{0}}$,故D正确.
故选D.
点评 本题以图象的形式考查了影响水的电离平衡的因素、弱电解质的电离、pH的简单计算等,题目难度中等,需要学生具有扎实的基础知识与读图获取信息的能力.


科目:高中化学 来源: 题型:填空题
 (代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示:
 的名称1,2-二甲苯(或邻二甲苯),D中官能团的名称为醛基,DMP的分子式为C10H10O4.
的名称1,2-二甲苯(或邻二甲苯),D中官能团的名称为醛基,DMP的分子式为C10H10O4.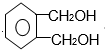 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$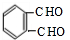 +2H2O.
+2H2O. .
. 制备DMP的另一种途径:
制备DMP的另一种途径:
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合物中CuO和Fe2O3的物质的量的比为1:1 | |
| B. | 参加反应的CO的质量为11.2g | |
| C. | 原混合物中Fe元素的质量为5.6g | |
| D. | 原混合物中CuO的质量分数约为33.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲、乙、丙、丁 | B. | 乙、甲、丙、丁 | C. | 乙、甲、丁、丙 | D. | 丁、丙、乙、甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 有机物A是一种重要的工业原料,其结构简式如图:
有机物A是一种重要的工业原料,其结构简式如图:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用碘水鉴别淀粉溶液和蔗糖溶液 | |
| B. | 用酸性高锰酸钾溶液鉴别乙烯和乙炔 | |
| C. | 用溴水鉴别四氯化碳和苯两种无色液体 | |
| D. | 用金属钠鉴别乙醇与二甲醚(CH3OCH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
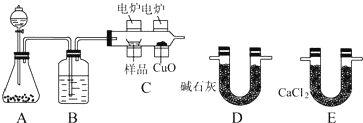
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 20℃ | 铁片 | 1mol/L硫酸 | B | 30℃ | 铁粉 | 1mol/L稀硫酸 |
| C | 30℃ | 铁粉 | 2mol/L稀硫酸 | D | 30℃ | 铁片 | 2mol/L稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com