
| 实验 | 实验现象 | 结 论 |
A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Cu>Fe |
B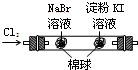 | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 白色固体先变为淡黄色,后变为黑色(Ag2S) | 溶解性:AgCl>AgBr>Ag2S |
D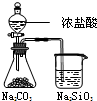 | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 酸性:HCl>H2CO3>H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.这两个原电池中,都是较活泼的金属作负极,较不活泼的金属作正极,正极上氢离子得电子生成氢气;
B.氯气和碘离子反应生成碘;
C.溶解性大的物质能转化为溶解性小的物质;
D.HCl也能和硅酸钠反应生成硅酸.
解答 解:A.这两个原电池中,都是较活泼的金属作负极,较不活泼的金属作正极,正极上氢离子得电子生成氢气,左边烧杯中铁为正极、右边烧杯中铜为正极,所以活动性:Al>Fe>Cu,故A错误;
B.和溴化钠反应的氯气能和碘化钾反应生成碘,从而造成干扰,所以不能Cl2>Br2>I2,故B错误;
C.溶解度大的物质能转化为溶解度小的物质,白色固体先变为淡黄色,说明AgCl变成了AgBr,后变为黑色Ag2S,即溶解性:AgCl>AgBr>Ag2S,故C正确;
D.依据强酸制弱酸的原理,锥形瓶中有气体产生,说明盐酸的酸性比碳酸强,浓盐酸易挥发,氯化氢和二氧化碳都进入硅酸钠溶液,不能证明产生的硅酸沉淀一定是二氧化碳反应的结果,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及酸性强弱比较、溶解度大小比较、氧化性强弱比较、金属性强弱比较等知识点,明确实验原理、物质性质是解本题关键,注意D中HCl、B中氯气对实验的干扰,为易错点.


科目:高中化学 来源: 题型:选择题
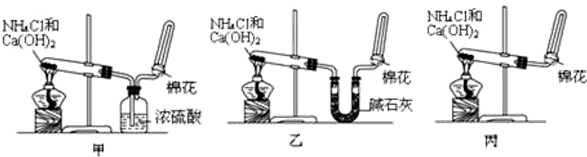
| A. | 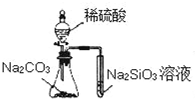 实验可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. | 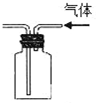 实验装置排空气法收集CO2气体 | |
| C. | 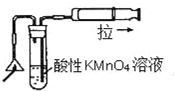 可以检验火柴燃烧生成的SO2气体 | |
| D. | 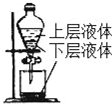 提取海带中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
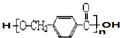 其合成路线如下:
其合成路线如下: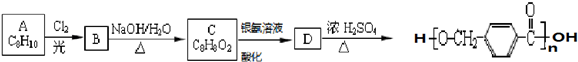
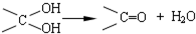
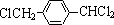 ,其中的官能团名称为氯原子.
,其中的官能团名称为氯原子.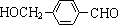 +2Ag(NH3)2OH $\stackrel{△}{→}$
+2Ag(NH3)2OH $\stackrel{△}{→}$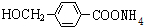 +2Ag↓+3NH3+H2O.由D生成高分子化合物的反应n
+2Ag↓+3NH3+H2O.由D生成高分子化合物的反应n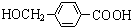 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$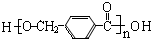 +(n-1)H2O.
+(n-1)H2O.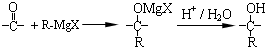
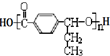 ,在合成过程中所用的格氏试剂的化学式为CH3CH2MgX(用X表示卤原子),合成过程中涉及到的有机化学反应类型有ACD(填编号)
,在合成过程中所用的格氏试剂的化学式为CH3CH2MgX(用X表示卤原子),合成过程中涉及到的有机化学反应类型有ACD(填编号)查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.0g甲醛和甲酸甲酯的混合物中含有的原子数为0.4NA | |
| B. | 常温下,1L0.1mol•L-1CuSO4溶液中粒子总数小于0.2NA | |
| C. | 1 mol冰醋酸和1 mol乙醇在浓硫酸加热下充分反应生成H2O个数为NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | R | X | Y | W |
| 原子半径/nm | 0.077 | 0.074 | 0.186 | 0.099 |
| 主要化合价 | +4、-4 | -2 | +1 | +7、-1 |
| A. | 简单的离子半径由小到大排序:Y、X、W | |
| B. | X的气态氢化物的稳定性一定比R的强 | |
| C. | R、X和Y可以组成含共价键的离子化合物 | |
| D. | 在R、X、W的氢化物中,X的沸点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子排布式为:1s22s22p63s23p63d34s2 | |
| B. | 该元素为VB | |
| C. | 元素为ⅢB族元素 | |
| D. | 该元素属于过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
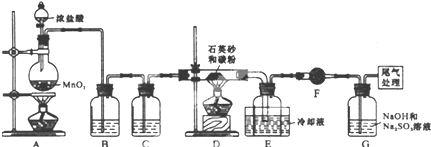
| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4(或溴水)溶液 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红溶液 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 假设2成立 | ||
| ③ | 向C试管中滴加几滴淀粉-KI溶液 | 若溶液变为蓝色 | 假设3成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com