
| A. | NA个Fe(OH)3胶体粒子的质量为107 g | |
| B. | 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA | |
| D. | 1 mol Na2O2固体中含离子总数为4NA |
分析 A、一个胶粒是多个氢氧化铁的聚集体;
B、Cu2S的摩尔质量是CuO的2倍,含有的铜原子个数也是CuO的2倍;
C、氯气和水的反应为可逆反应;
D、过氧化钠由2个钠离子和1个过氧根构成.
解答 解:A、一个胶粒是多个氢氧化铁的聚集体,故NA个氢氧化铁胶粒中氢氧化铁的物质的量大于1mol,则质量多于107g,故A错误;
B、Cu2S的摩尔质量是CuO的2倍,含有的铜原子个数也是CuO的2倍,故混合物可以看做由CuO构成,则8.0g混合物中含有的CuO的物质的量为0.1mol,则含铜原子为0.1NA个,故B正确;
C、氯气和水的反应为可逆反应,不能进行彻底,且生成的HClO会部分电离,故所得溶液中的HClO分子个数小于0.1NA个,故C错误;
D、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含离子共3NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:选择题
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O4 2NO2△H>0)
2NO2△H>0)
(a)将两容器置于沸水中加热;
(b)在活塞上都加2kg的砝码。
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
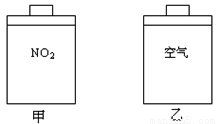
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ”或“
”或“ ”表示化学键断裂处,“
”表示化学键断裂处,“ ”表示生成的化学键( )
”表示生成的化学键( )| A. | 乙醇催化氧化: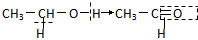 | B. | 乙酸和乙醇的酯化反应: | ||
| C. | 溴乙烷的消去反应: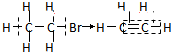 | D. | 乙醛的还原反应: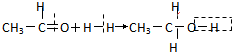 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电镀铜时用待镀的金属制品作阳极、铜作阴极 | |
| B. | AlCl3熔点低,电解熔融AlCl3冶炼铝更节能 | |
| C. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| D. | 氯碱工业实际是指电解饱和食盐水的工业生产 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
配制物质的量浓度为0.1 mol/L的Na2CO3溶液l00mL时,下列操作正确的是( )
A. 用托盘天平称取l.06g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 定容时,若仰视,则所配溶液的浓度将偏高
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com