
【题目】X、Y、Z、P、Q为周期表前四周期中原子序数依次增大的元素。X原子2p能级有两个未成对电子,但没有空轨道。Y原子K层的电子数与M层的电子数的乘积等于其L层的电子数。Z与X同族。P原子的基态+2价阳离子的价电子排布为3d2。Q位于第ⅠB族。根据以上信息,回答下列问题。
(1)X的基态原子核外有 种不同运动状态的电子。
(2)Y与X可以形成多种复杂阴离子,如图所示,若其中a对应的阴离子化学式为SiO44—,则c对应的阴离子的化学式为 。
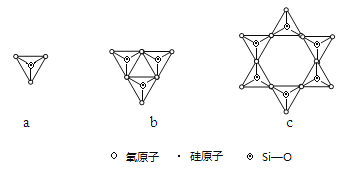
(3)Z能形成很多种含氧酸,如H2ZO3、H2ZO4。Z的某种含氧酸分子式为H2Z2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式 (配位键须注明)。
(4)P与X形成的某种晶体的晶胞结构如图所示,其晶体的化学式为 ,P的配位数为 。
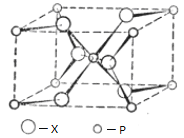
(5)向盛有QZX4的溶液中加入氨水至过量,现象为 ,相关反应的离子方程式为 。NF3的空间构型是 ,NF3不易与Cu2+形成配离子,其原因是 。
【答案】(1)8;(2)Si6O1812—(3) (4)TiO2;6
(4)TiO2;6
(5)先形成蓝色沉淀,氨水过量时,沉淀溶解,得到深蓝色的透明溶液;Cu2++2NH3﹒H2O = Cu(OH)2↓+ 2NH4+,Cu(OH)2+4NH3= [Cu(NH3)4]2++ 2OH—;三角锥形;NF3分子中氟原子电负性大,非金属性强,有吸电子效应,使得氮原子上的孤电子对难于与Cu2+形成配位键。
【解析】试题分析:X、Y、Z、P、Q为周期表前四周期中原子序数依次增大的元素。X原子2p能级有两个未成对电子,但没有空轨道,X为O元素。Y原子K层的电子数与M层的电子数的乘积等于其L层的电子数,M层的电子数为4,Y为Si元素。Z与X同族,Z为S元素。P原子的基态+2价阳离子的价电子排布为3d2,P为22号元素,是Ti元素。Q位于第ⅠB族,Q为Cu元素。
(1)X为O元素,核外有8个电子,基态原子核外有8种不同运动状态的电子,故答案为:8;
(2)Si与O可以形成多种复杂阴离子,若其中a对应的阴离子化学式为SiO44—,则c对应的阴离子含有Si原子数=6,O原子数为6×(2+2×![]() )=18,根据化合价的代数和等于离子所带电荷数,该离子带12个单位的负电荷,化学式为Si6O1812—,故答案为:Si6O1812—;
)=18,根据化合价的代数和等于离子所带电荷数,该离子带12个单位的负电荷,化学式为Si6O1812—,故答案为:Si6O1812—;
(3)S能形成很多种含氧酸,如H2SO3、H2SO4。Z的某种含氧酸分子式为H2S2O7,属于二元酸,其结构中所有原子都达到稳定结构,且不存在非极性键,其结构式为 ,故答案为:
,故答案为: ;
;
(4)Ti原子数为8×![]() +1=2,O原子数为2+4×
+1=2,O原子数为2+4×![]() =4,该晶体的化学式为TiO2;与Ti原子最近且距离相等的O原子数为6,即Ti的配位数为6,故答案为:TiO2;6;
=4,该晶体的化学式为TiO2;与Ti原子最近且距离相等的O原子数为6,即Ti的配位数为6,故答案为:TiO2;6;
(5)向盛有CuSO4的溶液中加入氨水至过量,可以看到先形成蓝色沉淀,氨水过量时,沉淀溶解,得到深蓝色的透明溶液,相关反应的离子方程式为Cu2++2NH3﹒H2O = Cu(OH)2↓+ 2NH4+,Cu(OH)2+4NH3= [Cu(NH3)4]2++ 2OH—;NF3中N原子上连接有3个原子,含有1个孤电子对,采用sp3杂化,空间构型是三角锥形;NF3分子中氟原子电负性大,非金属性强,有吸电子效应,使得氮原子上的孤电子对难于与Cu2+形成配位键。故答案为:先形成蓝色沉淀,氨水过量时,沉淀溶解,得到深蓝色的透明溶液;Cu2++2NH3﹒H2O = Cu(OH)2↓+ 2NH4+,Cu(OH)2+4NH3= [Cu(NH3)4]2++ 2OH—;三角锥形;NF3分子中氟原子电负性大,非金属性强,有吸电子效应,使得氮原子上的孤电子对难于与Cu2+形成配位键。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修2:化学与技术]辉铜矿主要成分为Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,以及少量SiO2、Fe2O3等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰晶体和碱式碳酸铜。主要工艺流程如下:
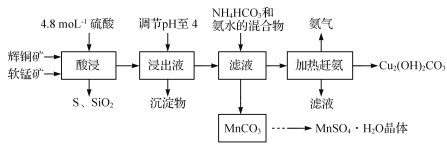
已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4
④MnSO4·H2O溶于1份冷水、0.6份沸水,不溶于乙醇。
(1)实验室配制250 mL 4.8 mol·L1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要 。
(2)酸浸时,为了提高浸取率可采取的措施有 (任写一点)。得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式: 。
(3)调节浸出液pH=4的作用是 。
(4)本工艺中可循环使用的物质是 (写化学式)。
(5)获得的MnSO4·H2O晶体需要进一步洗涤、干燥,洗涤时应用 洗涤。
(6)测定MnSO4·H2O样品的纯度:准确称取样品14.00 g,加蒸馏水配成100 mL溶液,从中取出25.00 mL用标准的BaCl2溶液测定,完全反应后得到了4.66 g沉淀,则此样品的纯度为__________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述正确的是( )
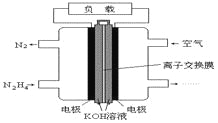
A. 电子从右侧电极经过负载后流向左侧电极
B. 负极发生的电极反应式为:N2H4- 4e-=N2+4H+
C. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D. 该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是生产塑料和合成橡胶的重要基本有机原料,乙苯催化脱氢法是目前国内外生产苯乙烯的主要方法,其化学方程式为:
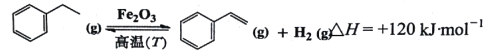
(1)升高反应温度,其转化率________,反应速率________(填“增大”、“减小”或“不变”)。
(2)等温、等压下,通入惰性气体(如水蒸气)能提高反应的转化率,其原因是________。
(3)通入水蒸气可延续催化剂Fe2O3被还原而失活,其原因是________(用化学平衡原理解释)。
(4)一定条件下,在体积不变的密闭容器中,反应过程中各物质浓度随时间变化的关系如下图所示。在t1时刻加入H2,t2时刻再次达到平衡。回答下列问题:
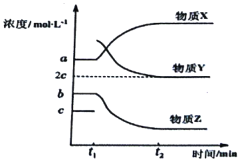
①物质X为__________,判断理由是__________;
②t2时刻,苯乙烯的浓度为______molL-1;
③t1-t2时间段内,乙苯的反应速率为_______molL-1min-1;
(5)温度T下,已知H2和苯乙烯的燃烧热△H分别为-290kJmol-1和-4400kJmol-1,则乙苯的燃烧热为△H_______kJmol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工业生产和国防建设中有广泛应用。回答下列问题:
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程:
。
(2)联氨(N2H4)是一种还原剂。已知:H2O(l)=H2O(g) △H=+44kJ/mol。试结合下表数据,写出N2H4 (g)燃烧热的热化学方程式: 。
化学键 | N—H | N—N | N=N | N≡N | O=O | O—H |
键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(3)KCN可用于溶解难溶金属卤化物。将AgI溶于KCN溶液中,形成稳定的Ag(CN)2—,该转化的离子方程式为: 。若已知Ksp(AgI)=1.5×10—16,K稳[Ag(CN)2—]=1.0×10-21,则上述转化方程式的平衡常数K= 。(提示:K稳越大,表示该化合物越稳定)
(4)氨的催化氧化用于工业生产硝酸。该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式: 。
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2![]()
![]() N2O4其相关图像如下。
N2O4其相关图像如下。

①0~3s时v(NO2)增大的原因是 。
②5s时NO2转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e五种短周期元素的原子序数逐渐增大。a为非金属元素,且a、e同主族,c、d为同周期的相邻元素。e原子的质子数等于c、d原子最外层电子数之和。b原子最外层电子数是内层电子数的2倍。c的气态氢化物分子中有3个共价键。试推断:
(1)写出b元素在周期表中的位置 ;
(2)写出一种由a、c、d所形成的离子化合物 (化学式),它与e的最高价氧化物对应水化物的溶液加热时反应的离子方程式是 ;
(3)c的单质的电子式为 。
(4)b的最简单气态氢化物的结构式是
(5)b和d相比,非金属性较强的是 (用元素符号表示),下列事实能证明这一结论的是 (选填字母序号)。
A.常温下,b的单质呈固态,d的单质呈气态 |
B.d的氢化物的稳定性强于b的氢化物 |
C.b与d形成的化合物中,b呈正价 |
D.d的氢化物的沸点高于b的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)下图为四种粒子的结构示意图,完成以下填空:
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
属于阳离子结构的粒子是________(填字母序号,下同);A粒子的半径________B粒子的半径(填“>”、“<”或“=”)。
(2)有机物M经过太阳光光照可转化成N,转化过程如下:

![]()
 ΔH = +88.6 kJ·mol-1
ΔH = +88.6 kJ·mol-1
则M、N相比,较稳定的是____________。
(3) 由氢气和氧气反应生成1 mol水蒸气放出热量241.8 kJ,写出该反应的热化学方程式为:_____________________________________________________。
(4)一定温度下在某定容容器中发生反应:2A(g)+3B(g)![]() 2C(g),开始时,A的浓度为2 mol·L-1,B的浓度为4 mol·L-1,2 min后,A的浓度减少0.8 mol·L-1,则
2C(g),开始时,A的浓度为2 mol·L-1,B的浓度为4 mol·L-1,2 min后,A的浓度减少0.8 mol·L-1,则
① v(B)=____________,v(C)=__________。
② 在2 min末,C的浓度是__________,B的浓度是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备溴苯的实验装置如下图,将液溴从恒压滴液漏斗慢慢滴入盛有苯和铁粉的烧瓶A。反应结束后,对A中的液体进行后续处理即可获得溴苯。

(1)写出A中制备溴苯的化学反应方程式 。
(2)B中盛放的CCl4的作用是 。
(3)冷凝管的作用是 ,冷凝管中的水应从 口进入(填“a”或“b”)。
(4)向C中加入硝酸银溶液可证明苯和液溴发生的是取代反应而不是加成反应,反应现象是 ,也可使用 试纸更简便地证明上述结论。
(5)得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗,正确的操作顺序是 (填字母标号)。
a.①②③④② b.②④②③① c.④②③①② d.②④①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】IA、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构。

(1)试判断A、B、C、D四种元素的名称。A______,B_____,C______,D______。
(2)C在周期表中的位置是 。
(3)由B、D两种元素组成的D2B2型化合物的电子式为_______,CB2的电子式 为________。
(4)如右图所示,在烧瓶中收集满CB2气体,用带导管(导管一端事先绑好一个气球)的胶塞紧,当打开胶塞迅速倒入浓的A、B、D三种元素组成的化合物的溶液后,立即塞紧胶塞振荡,可观察到_____,原因是_____________。
II(9分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
主族K] | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | [m] | ⑩ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的分子式是: ,碱性最强的化合物的电子式是: 。
(2)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式 。
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式 ,该化合物是由 (填“极性”“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______(要求用离子符号表示)。
(6)元素③的氢化物常温下和元素⑦的单质反应的离子方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com