
【题目】工业制硫酸在接触室中发生的主要反应为2SO2(g)+O2(g)![]() 2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:
2SO3(g)。在一定温度下,向2L密闭容器内投入4molSO2(g)和2molO2(g)发生上述反应,n(SO2)随时间的变化如表所示:
时间(s) | 0 | 1 | 2 | 3 | 5 |
n(SO2)(mol) | 4 | 3.2 | 1.6 | 1.4 | 1.4 |
(1)用SO3表示从0~2s内该反应的平均速率v(SO3)=___。
(2)该反应达到最大限度时SO2的转化率为___。
(提示:转化率=![]() ×100%)
×100%)
(3)该反应达到最大限度时O2的浓度为___。
(4)下列叙述能说明上述反应达到平衡状态的是___。
A.容器内压强保持不变
B.v(SO2)=2v(O2)
C.SO3的浓度不再变化
D.SO2、O2、SO3为浓度之比为2∶1∶2
E.单位时间内每消耗2molSO2,同时生成2molSO3
【答案】0.6mol/(Ls) 65% 0.35mol/L AC
【解析】
(1)0~2s内△n(SO2)=4mol-1.6mol=2.4mol,根据方程式2SO2(g)+O2(g)![]() 2SO3(g)可知该时间段内△n(SO3)=2.4mol,容器体积为2L,所以v(SO3)=
2SO3(g)可知该时间段内△n(SO3)=2.4mol,容器体积为2L,所以v(SO3)=![]() = 0.6mol/(Ls);
= 0.6mol/(Ls);
(2)根据表格可知3s后二氧化硫浓度不在改变,说明此时反应已经达到平衡,此时二氧化硫的转化率为![]() =65%;
=65%;
(3)平衡时△n(SO2)=2.6mol,根据方程式可知△n(O2)=1.3mol,则剩余氧气的物质的量为2mol-1.3mol=0.7mol,容器体积为2L,所以c(O2)=![]() =0.35mol/L;
=0.35mol/L;
(4)A.容器体积恒定,平衡正向移动时气体的物质的量减小,容器内压强减小,所以当压强不变时说明反应达到平衡,故A正确;
B.未指明正反应速率还是逆反应速率,故B错误;
C.反应达到平衡时,各物质的浓度不再改变,所以三氧化硫浓度不再变化说明反应达到平衡,故C正确;
D.平衡时各物质的浓度不再改变,但比值不一定,与转化率有关,故D错误;
E.只要反应进行单位时间内每消耗2molSO2,就会同时生成2molSO3,故E错误;
综上所述答案为AC。


科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
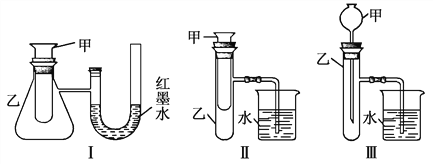
(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是___________________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是___________________,说明该反应属于___________________(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是___________________;
②若观察到烧杯里产生气泡,则说明M溶于水___________________ (填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”),理由是___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤和石油不仅是重要的矿物能源,更可以通过综合利用得到多种有机化工产品。煤干馏后可得到焦炭、煤焦油、粗氨水和焦炉气等。焦炭可通过以下途径制取聚氯乙烯等化工产品。
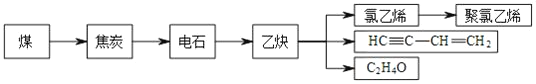
完成下列填空:
(1)石油化工生产乙烯的操作名称为___,实验室制取乙烯的反应条件是___,乙炔的分子空间构型是____,由乙炔生产HC≡C-CH=CH2的基本反应类型是___。在石油生产乙烯的过程中会产生副产品异戊烯,通过催化脱氢法得到异戊二烯,进而的到异戊橡胶,由异戊二烯生产异戊橡胶的化学方程式为:___。
(2)检验C2H4O中是否含有醛基的实验方法是___;其中涉及的化学反应方程式为____。
(3)乙炔可用来合成聚氯乙烯。请以乙烯为原料,无机试剂任选,设计聚氯乙烯的合成路线。____
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用图1实验装置测定锌与稀硫酸反应的速率。
(1)检查图1装置气密性的操作方法是_____。
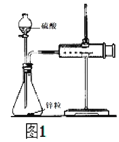
(2)分别取2g颗粒大小相同的锌粒分别与体积均为40mL的1mol/L硫酸、4mol/L硫酸反应,收集25mLH2时所需时间后者比前者_____。(填“长”或“短”)
(3)同学们在实验操作中发现本实验设计存在明显不足,例如_____。
(4)某化学兴趣小组对教材实验装置进行图2所示改进。检查装置气密性后进行的实验操作有:_____。
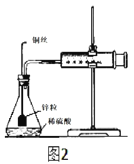
a.在多孔塑料袋中装入锌粒
b.在锥形瓶中加入40mL1mol/L硫酸
c.塞好橡胶塞,时立即用秒表计时
d.注射器内每增加5mL气体时读取一次秒表
(5)实验观察到锌与稀硫酸反应初期速率逐渐加快,其原因是_____,反应进行一定时间后速率逐渐减慢,原因是_____。
(6)测得产生H2的体积与反应时间的关系曲线如图3所示,t1~t2时间段氢气体积略有减小的原因是_____;在64s内用H+浓度表示的平均反应速率v(H+)=______(此时,溶液体积仍为40mL,气体摩尔体积25L/mol)。
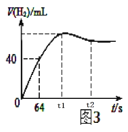
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式为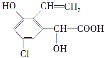 ,下列关于该有机物的说法中不正确的是
,下列关于该有机物的说法中不正确的是
A. 遇FeCl3溶液显紫色
B. 与足量的氢氧化钠溶液在一定条件下反应,最多消耗NaOH 3 mol
C. 能发生缩聚反应和加聚反应
D. 1 mol该有机物与浓溴水反应,最多消耗3 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___,形成的单质是半导体的是___(填元素名称)。
(2)⑥与⑨形成的化合物的电子式为___,①与②形成的最简单化合物的结构式为___。
(3
(4)气态氢化物最稳定的是___(填化学式),②、③、⑧的原子半径最小是__(填素符号)。
(5)④与⑧形成的化合物的属于___(填“离子化合物”或“共价化合物”),该晶体属于___晶体(填“离子”、“分子”、“原子”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究原电池产生电流的过程,设计了如图所示实验:
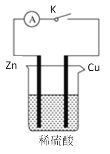
(1)下列叙述中正确的是___。
A.打开开关K时铜片作负极,关闭开关K时铜片作正极
B.打开开关K,锌片和铜片上均有气泡产生
C.关闭开关K后,溶液中的H+浓度减小
D.关闭开关K产生气泡的速率比打开开关K时慢
(2)打开开关K后,装置中发生反应的离子方程式为___。
(3)关闭开关K后,则该装置为___(填“原电池”或“电解池”),锌极为___极(填“正”、“负”、“阳”或“阴”),铜极上的电极反应式为__。若反应过程中有0.3mol的电子发生转移,则产生的气体在标准状况下的体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是( )
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.ClO2作水处理剂时,利用了其强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为短周期元素且原子序数依次増大,质子数之和为40。B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E的最高价氧化物的水化物呈两性。
(1)B元素在周期表中的位置为_______。
(2)由A、C、D三种元素组成的化合物的电子式为_______。
(3)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。現改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式______。
(4)若BA3与C2可形成燃料电池,电解质为KOH溶液,则负极的电极反应式为______。(氧化产物不污染环境)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com