
| A£® | SO2ŗĶNaOH | B£® | CO2ŗĶH2O | C£® | Cl2ŗĶHCl | D£® | CCl4ŗĶNaCl |
·ÖĪö Ņ»°ćĄ“Ėµ£¬»īĘĆ½šŹōŗĶ»īĘĆ·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³ÉĄė×Ó¼ü£¬²»Ķ¬·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³É¼«ŠŌ¼ü£¬Ķ¬ÖÖ·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³É·Ē¼«ŠŌ¼ü£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®SO2ÖŠÖ»ÓŠ¹²¼Ū¼ü£¬NaOHÖŠ“ęŌŚĄė×Ó¼üŗĶ¹²¼Ū¼ü£¬¹ŹA“ķĪó£»
B£®CO2ŗĶH2OÖŠ¶¼Ö»“ęŌŚ¼«ŠŌ¹²¼Ū¼ü£¬¹ŹBÕżČ·£»
C£®Cl2·Ö×ÓÖŠClŌ×ÓÖ®¼ä“ęŌŚ·Ē¼«ŠŌ¼ü£¬HClÖŠ“ęŌŚ¼«ŠŌ¹²¼Ū¼ü£¬¹ŹC“ķĪó£»
D£®CCl4ÖŠÖ»“ęŌŚ¼«ŠŌ¹²¼Ū¼ü£¬NaClÖŠÖ»“ęŌŚĄė×Ó¼ü£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ¼üµÄÅŠ¶Ļ£¬Ć÷Č·ĪļÖŹµÄ¹¹³ÉĪ¢Į£ÅŠ¶Ļ»Æѧ¼ü¼“æÉ£¬ÖŖµĄÄÄŠ©ŌŖĖŲŅ׊Ī³ÉĄė×Ó¼ü£¬×¢ŅāĻ”ÓŠĘųĢåÖŠ²»“ęŌŚ»Æѧ¼ü£¬ĪŖŅדķµć£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Éś²ś¹ż³Ģ֊ƻӊÉę¼°µ½Ńõ»Æ»¹Ō·“Ó¦ | |
| B£® | Éś²ś¹ż³Ģ֊ƻӊÉę¼°µ½ÖĆ»»·“Ó¦ | |
| C£® | øĆ³§Éś²śµÄÖ÷ŅŖŌĮĻĪŖĆŗ”¢“æ¼ī | |
| D£® | øĆ³§Éś²śµÄ×īÖÕ²śĘ·ŹĒŠ”ĖÕ“ņ¼°ÉÕ¼ī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģå»ż | B£® | Ō×ÓøöŹż | C£® | ÖŹĮæ | D£® | µē×ÓŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ${\;}_{17}^{35}$Cl2Óė${\;}_{17}^{37}$Cl2Ńõ»ÆÄÜĮ¦Ļą½ü£¬¶žÕß»„ĪŖĶ¬Ī»ĖŲ | |
| B£® | .¹żŃõ»ÆĒāµÄµē×ÓŹ½£ŗ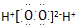 | |
| C£® | .Ķ¬Ö÷×åŌŖĖŲŠĪ³ÉµÄŗ¬ŃõĖįµÄĖįŠŌĖęŗĖµēŗÉŹżµÄŌö¼Ó¶ų¼õČõ | |
| D£® | .Ķ¬ÖÜĘŚÖ÷×åŌŖĖŲŌ×Ó°ė¾¶ĖęŗĖµēŗÉŹżµÄŌö“ó¶ų¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśÓėŃĪĖį·“Ó¦£¬ĢśŗĻ½š²»ÓėŃĪĖį·“Ó¦ | |
| B£® | Ņ»¶ØĢõ¼žĻĀ£¬Ģś·ŪæÉÓėĖ®ÕōĘų·“Ӧɜ³ÉĖÄŃõ»ÆČżĢśŗĶĒāĘų | |
| C£® | ²»ŠāøÖŹĒĢśŗĻ½š£¬Ö»ŗ¬½šŹōŌŖĖŲ | |
| D£® | “æĢśµÄÓ²¶ČŗĶČŪµć¾łµĶÓŚĢśŗĻ½š |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | S2ŗĶS8µÄ»ģŗĻĪļ¹²6.4 g£¬Ėłŗ¬ĮņŌ×ÓŹżŅ»¶ØĪŖ0.2NA | |
| B£® | ½«100 mL 0.1 mol•L-1µÄFeCl3ČÜŅŗµĪČė·ŠĖ®ÖŠæÉÖʵĆFe£ØOH£©3½ŗĮ£ŹżÄæĪŖ0.01NA | |
| C£® | ŌŚ·“Ó¦KClO3+6HClØTKCl+3Cl2”ü+3H2OÖŠ£¬ĆæÉś³É3 mol Cl2£¬×ŖŅʵĵē×ÓŹżĪŖ6NA | |
| D£® | ½«ŗ¬ÓŠ1 mol Na2CO3µÄČÜŅŗÖšµĪ¼ÓČėµ½ŗ¬1.5 mol HClµÄČÜŅŗÖŠ£¬²śÉśĘųĢåµÄ·Ö×ÓŹżÄæĪŖ0.5NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2”¢SiO2µÄ¾§Ģå½į¹¹ĄąŠĶ²»Ķ¬ | |
| B£® | ¼ÓČČ¹č”¢Įņ¾§ĢåŹ¹Ö®ČŪ»Æ£¬æĖ·žµÄ×÷ÓĆĮ¦²»Ķ¬ | |
| C£® | HF±ČHClĪČ¶ØŹĒŅņĪŖHF¼ä“ęŌŚĒā¼ü | |
| D£® | NaOH”¢NH4Cl¾§ĢåÖŠ¼ČÓŠĄė×Ó¼üÓÖÓŠ¹²¼Ū¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
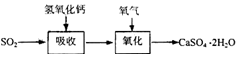
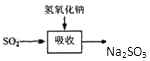
| ŹŌ¼Į | Ca£ØOH£©2 | NaOH |
| ¼Ūøń£ØŌŖ/kg£© | 0.36 | 2.9 |
| ĪüŹÕSO2µÄ³É±¾£ØŌŖ/mol£© | 0.027 | 0.232 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com