
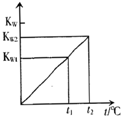
 Ė®µÄĄė×Ó»ż³£ŹżKWÓėĪĀ¶Čt£Ø”ę£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
Ė®µÄĄė×Ó»ż³£ŹżKWÓėĪĀ¶Čt£Ø”ę£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ·ÖĪö £Ø1£©ŌŚ25”ę£¬ŌņKw=10-14£¬øł¾ŻpH=-lgc£ØH+£©¼ĘĖćpH£»
£Ø2£©øł¾Ż0.1L 0.1mo/LµÄNaAČÜŅŗµÄpH=10ÅŠ¶ĻŃĪµÄĄąŠĶ£¬Č·¶Ø“ęŌŚµÄĘ½ŗā£¬±Č½ĻĄė×ÓÅØ¶ČµÄ“óŠ”£»
£Ø3£©Éč³öĒāŃõ»ÆÄĘČÜŅŗĪŖxŗĶĮņĖįČÜŅŗµÄĢå»żĪŖy£¬øł¾ŻĢāÖŠŹż¾ŻĮŠŹ½¼ĘĖć³öĢå»żÖ®±Č£»
£Ø4£©Éč³öĖįČÜŅŗµÄpHĪŖa£¬¼īČÜŅŗµÄpHĪŖb£¬øł¾Ż100”ꏱ¼°Ģå»ż¹ŲĻµĮŠŹ½¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©ŌŚ25”ę£¬ŌņKw=10-14£¬øł¾ŻpH=-lgc£ØH+£©=-lg$\frac{1{0}^{-12}}{0.1}$=11£¬¹Ź“š°øĪŖ£ŗ10-14£»11£»
£Ø2£©ÓÉÓŚ0.1L 0.1mo/LµÄNaAČÜŅŗµÄpH=10£¬ĖµĆ÷ČÜŅŗĻŌŹ¾¼īŠŌ£¬ŹōÓŚĒæ¼īČõĖįŃĪ£¬“ęŌŚĘ½ŗāA-+H2O?HA+OH-£¬H2O?H++OH-£¬¹Ź²»Ė®½āµÄÄĘĄė×ÓÅØ¶Č“óÓŚA-Ąė×ÓÅØ¶Č£¬ČÜŅŗĻŌ¼īŠŌ£¬ĒāĄė×ÓÅØ¶Č“óÓŚĒāŃõøłĄė×ÓÅØ¶Č£¬
¹Ź“š°øĪŖ£ŗA-+H2O?HA+OH-£¬H2O?H++OH-£»c£ØNa+£©£¾c£ØA-£©£¾c£ØOH-£©£¾c£ØH+£©£»
£Ø3£©ÉčĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĪŖxL£¬ĮņĖįČÜŅŗµÄĢå»żĪŖyL£¬pH=11µÄNaOHČÜŅŗÖŠ£¬ĒāŃõøłĄė×ÓµÄÅضČĪŖ£ŗ10-3mol/L£¬pH=4µÄĮņĖįČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ£ŗ10-4mol/L£¬
¶žÕß»ģŗĻŗóČÜŅŗµÄpH=9£¬ČÜŅŗĖįŠŌ¼īŠŌ£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓµÄÅضČĪŖ10-5mol/L£¬¼“ĒāŃõ»ÆÄĘ¹żĮ棬¼“10-3mol/L”ĮxL-10-4mol/L”Įy=10-5mol/L£Øx+y£©£¬
½āµĆx£ŗy=1£ŗ9£¬
¹Ź“š°øĪŖ£ŗ1£ŗ9£»
£Ø4£©ÉčĒæĖįČÜŅŗµÄpHĪŖa£¬Ģå»żĪŖ10V£¬ČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ£ŗ10-amol/L£»¼īČÜŅŗµÄpHĪŖb£¬Ģå»żĪŖV£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓµÄÅضČĪŖ£ŗ10-£Ø12-b£©mol/L£¬
»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£¬ŌņĀś×ćČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæ“óÓŚĒāŃõøłĄė×ÓµÄĪļÖŹµÄĮ棬¼“10-amol/L”Į10VL=10-£Ø12-b£©mol/L”ĮVL£¬
½āµĆ£ŗ1-a=b-12£¬a+b=13£¬
¹Ź“š°øĪŖ£ŗ13£®
µćĘĄ ±¾Ģāæ¼²éĮĖĖ®µÄµēĄėĘ½ŗā·ÖĪö£¬Ąė×Ó»ż³£ŹżµÄ¼ĘĖćÓ¦ÓĆ£¬×¢ŅāĄė×Ó»żŹĒŅ»¶ØĪĀ¶ČĻĀµÄ³£Źż£¬ĖęĪĀ¶Čøı䣬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
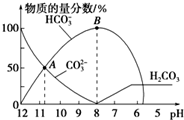
| A£® | ŌŚAµćĖłŹ¾µÄČÜŅŗÖŠ£ŗc£ØNa+£©+c£ØH+£©=2c£ØCO32-£©+c£ØHCO3-£©+c£ØOH-£© | |
| B£® | ŌŚBµćĖłŹ¾µÄČÜŅŗÖŠ£¬ÅضČ×ī“óµÄĄė×ÓŹĒNa+ | |
| C£® | µ±ČÜŅŗµÄpHĪŖ7Ź±£¬ČÜŅŗµÄ×ÜĢå»ż“óÓŚ20mL | |
| D£® | 25”ꏱ£¬CO32-Ė®½ā³£ŹżKh=2”Į10-4mol•L-1£¬µ±ČÜŅŗÖŠc£ØHCO3-£©£ŗc£ØCO32-£©=2£ŗ1Ź±£¬ČÜŅŗµÄpH=10 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 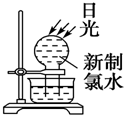 | B£® |  | ||
| C£® | 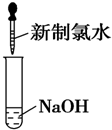 | D£® | 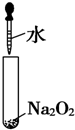 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCO3-”¢Ag+”¢NO3-”¢Na+ | B£® | Na+”¢Cl-”¢CO32-”¢NO3- | ||
| C£® | Fe3+”¢Na+”¢Cl-”¢SO42- | D£® | H+”¢Cl-”¢CO32-”¢NH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū¢ß¢ą¢į¢ā | B£® | ¢Ł¢Ś¢Ū¢Ż¢ą¢į | C£® | ¢Ś¢Ż¢Ž¢ß¢ą | D£® | ¢Ś¢Ü¢ß¢ą¢ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ±½±ūĖįŵĮś·Ö×Ó֊ƻӊŹÖŠŌĢ¼Ō×Ó | |
| B£® | ±½±ūĖįŵĮśŹōÓŚ·¼ĻćĢž | |
| C£® | ±½±ūĖįŵĮś¼ČÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗÓÖÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« | |
| D£® | 1mol±½±ūĖįŵĮś×ī¶ąæÉÓė2 molµÄNaOHČÜŅŗ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C3H6 | B£® | C2H4 | C£® | C4H6 | D£® | C2H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ūĻ©ŗĶ»·±ūĶé×é³ÉµÄ42 g»ģŗĻĘųĢåÖŠĒāŌ×ÓµÄøöŹżĪŖ6NA | |
| B£® | ±ź×¼×“æöĻĀ£¬4.48 L¼ŗĶéŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.2NA | |
| C£® | ±ź×¼×“æöĻĀ£¬6.72LNO2ÓėĖ®·“Ó¦ĻūŗĵÄŃõ»Æ¼Į·Ö×ÓŹżĪŖ0.2NA | |
| D£® | 1 mol OD-Ąė×Óŗ¬ÓŠµÄÖŹ×Ó”¢ÖŠ×ÓŹż¾łĪŖ10NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com