


 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��KOH | B��CaCl | C��H O O | D��NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaCl��HCl | B��MgCl2��SO2 |
| C��KCl ��CCl4 | D��CO2��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ۼ��ķ����� | B�����ۼ��ı����� |
| C�����ۼ��ļ��� | D�����ۼ��ļ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

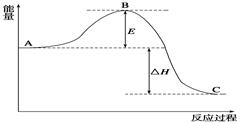
| A��CO2����ֽ�����CO����O2����ķ�Ӧ�Ƿ��ȷ�Ӧ |
| B��CO������O2��������CO2����ķ�Ӧ�Ƿ��ȷ�Ӧ |
| C����ͼ�ɱ�ʾ��CO��������CO2����ķ�Ӧ���̺�������ϵ |
| D������ͬ�����£�2 mol CO������1 mol O2����������ܺʹ���2 mol CO2��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������� | B�������ھƾ� | C��ʳ������ˮ | D����������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ʷ�����һ�����й��ۼ� |
| B���ɷǽ���Ԫ����ɵĻ����ﲻһ���ǹ��ۻ����� |
| C����ѧ�������ڵķ���֮��ǿ�ҵ������ |
| D������������ͨ�������������γɵĻ�ѧ���������Ӽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����κ����ʷ����ж����л�ѧ�� |
| B���γ����Ӽ����������Ӽ�ֻ���ھ��������� |
| C��D2O������H2O����������������������ȵķ��� |
| D��CO2��PCl3����������ԭ�Ӷ����������8�����ȶ��ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com