
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气, ![]() 减小
减小
B.通入少量SO2 , 溶液的漂白性增强
C.加入少量水,水的电离平衡向正反应方向移动
D.加入少量固体NaOH,一定有c(Na+)=c(Cl﹣)+c(ClO﹣)
【答案】C
【解析】解:在氯水中存在如下平衡:Cl2+H2O ![]() HCl+HClO、H2O
HCl+HClO、H2O ![]() H++OH﹣、HClO
H++OH﹣、HClO ![]() H++ClO﹣ . A.氯气溶于水达到平衡后,再通入少量氯气,此时已经为饱和溶液,浓度比值
H++ClO﹣ . A.氯气溶于水达到平衡后,再通入少量氯气,此时已经为饱和溶液,浓度比值 ![]() 不变,故A错误;
不变,故A错误;
B、通入少量SO2 , 发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,平衡左移,HClO的浓度减小,溶液漂白性减弱,故B错误;
C、加入少量水,促进水的电离,水的电离平衡向正反应方向移动,故C正确;
D、加入少量氢氧化钠,反应后溶液中阴阳离子所带正负电荷总数相等,故存在c(H+)+c(Na+)=c(OH﹣)+c(Cl﹣)+c(ClO﹣),加入少量固体NaOH,溶液呈酸性,则有:c(H+)>c(OH﹣),所以c(Na+)<c(Cl﹣)+c(ClO﹣),故D错误.
故选C.
A、氯气与水的反应,加入氯气,溶液为饱和溶液;
B、通入二氧化硫,其与氯气反应生成无漂白性的盐酸和硫酸,平衡左移,漂白性减弱;
C、氯气与水的反应,加入水,电离平衡向右移动;
D、根据电荷守恒可知:c(Na+)+c(H+)=c(Cl﹣))+c(ClO﹣)+c(OH﹣),加入少量固体NaOH,溶液呈酸性,只有溶液为中性时c(Na+)=c(Cl﹣)+c(ClO﹣).


科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示(部分物质和条件已略去),A是一种淡黄色粉末,B是某种矿物中的主要成分,D、Y是空气含量最多的两种气体,J是一种紫红色金属,X是最常见的无色液体. 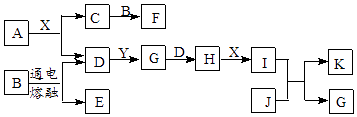
(1)A的化学式为
(2)Y的电子式为
(3)I与J反应的化学方程式为
(4)C与B在溶剂X中反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种微粒中的质子数和核外电子数都分别相同,那么这两种微粒不可能是( )
A.两种不同分子B.一种分子和一种离子
C.两种不同阴离子D.两种不同的阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式: ①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=﹣26.7kJmol﹣1
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=﹣50.75kJmol﹣1
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=﹣36.5kJmol﹣1
则反应FeO(s)+CO(g)═Fe(s)+CO2(g)的焓变为( )
A.+7.28 kJmol﹣1
B.﹣7.28 kJmol﹣1
C.+43.68 kJmol﹣1
D.﹣43.68 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、D、E、G四种微粒组成的复盐W的化学式为xAaDdyE2DzG.4.704g W溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g.同质量的W与5.13g氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,加热后的残渣用水充分溶解后过滤,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,滴定完毕后,溶液中检测不出任何金属离子和酸根离子;滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,依据推理和计算判断:
(1)依次写出D、E、G三种微粒符号、、;
(2)a、d的比值为;
(3)复盐的化学式为 . (写出计算步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为生活中的常见金属,C为磁性黑色晶体,A、B、C、D之间转化关系

(1)写出以下物质的化学式B_____________、C____________。
(2)C+盐酸→B+D的离子方程式为__________________________________,D的溶液可作为印刷电路板“腐蚀液”,写出该反应的化学方程式__________________________。
(3)实验室保存B的溶液时常加入少量A,原因是_________________(用离子方程式表示)
(4)向B溶液中滴加NaOH溶液,产生的现象是___________________________,过程中所发生的氧化还原反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等.某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2 , 其部分工艺流程如下: 
(1)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为 .
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是、 .
(3)该厂结合本厂实际,选用的X为(填化学式);中和Ⅰ使溶液中(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略).
(4)上述流程中洗涤的目的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com