
| A. | 用H2O2酸性溶液,将海带灰中的I-转变为I2:H2O2+2I-═I2+2OH- | |
| B. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 工业电解熔融氯化钠制金属钠:2Na++2Cl-$?_{熔融}^{电解}$2Na+Cl2↑ | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
分析 A.酸性条件下不生成OH-;
B、漂白粉溶液在空气中失效是因为次氯酸酸性比碳酸弱,次氯酸钙溶液中吸收二氧化碳反应生成碳酸钙和次氯酸;
C、工业电解熔融氯化钠制金属钠和氯气:
D、向Na2S2O3溶液中加入稀硫酸的离子反应为2H++S2O32-═S↓+SO2↑+H2O.
解答 解:A.用H2O2酸性溶液,将海带灰中的I-转变为I2的离子反应为2H++H2O2+2I-=I2+2H2O,故A错误;
B、次氯酸钙溶液中吸收二氧化碳反应生成碳酸钙和次氯酸,次氯酸见光分解失效,反应的离子方程式为:2ClO-+CO2+H2O+Ca2+═2HClO+CaCO3↓,故B错误;
C、工业电解熔融氯化钠制金属钠和氯气,电解的离子反应方程式为:2Na++2Cl-$?_{熔融}^{电解}$2Na+Cl2↑,故C正确:
D、向Na2S2O3溶液中加入稀硫酸,生成+4价的二氧化硫气体,所以反应的离子反应为2H++S2O32-═S↓+SO2↑+H2O,故D错误;
故选C.
点评 本题考查离子反应方程式的书写,为高频考点,涉及氧化还原,把握发生的化学反应及离子反应的书写方法为解答的关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 2个甲基,能生成4种-氯代物 | B. | 3个甲基,能生成5种-氯代物 | ||
| C. | 3个甲基,能生成9种-氯代物 | D. | 4个甲基,能生成4种-氯代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 气体 | 所用试剂 | 干燥剂 | 装置(可加热) | |
| A | O2 | 氯酸钾和二氧化锰 | 无水氯化钙 | 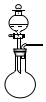 |
| B | NH3 | 浓氨水和生石灰 | 碱石灰 | |
| C | H2 | 稀硝酸和锌粒 | 浓硫酸 | |
| D | SO2 | 浓盐酸和亚硫酸钠 | 碱石灰 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 丙烷和2-甲基丙烷的一氯代物均为两种 | |
| C. | 油脂发生皂化反应能生成甘油 | |
| D. | 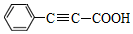 是高分子化合物 是高分子化合物 的单体 的单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
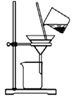
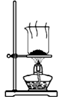
| A.制取氨气 | B.制取NaHCO3 | C.分离NaHCO3 | D.干燥NaHCO3 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶可防止食物受潮是由于其具有吸水性 | |
| B. | 持续加热到一定温度能杀死甲型H1N1流感病毒是因为病毒蛋白质受热变性 | |
| C. | 纤维素在人体内可水解为葡萄糖是人类重要的营养物质之一 | |
| D. | 酸性重铬酸钾用于检查酒驾是利用其强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com