
近年来,以天然气等为原料合成甲醇的难题被一一攻克,极大地促进了甲醇化学的发展。
(1)与炭和水蒸气的反应相似,以天然气为原料也可以制得CO和H2,该反应的化学方程式为_________。
(2)合成甲醇的一种方法是以CO和H2为原料,其能量变化如图所示:
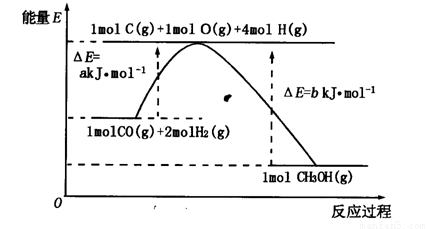
由图可知,合成甲醇的热化学方程式为________________________________________。
(3)以CO2为原料也可以合成甲醇,其反应原理为:CO2(g)+3H2(g)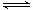 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①在lL的密闭容器中,充入1molCO2和3molH2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时问变化如图所示:
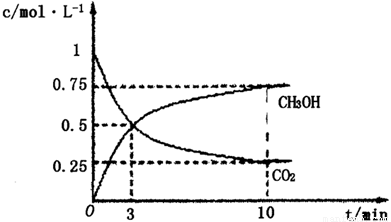
则下列说法正确的是_________________(填字母);
A.3min时反应达到平衡
B.0~10min时用H2表示的反应速率为0.225mol·-1·min-1
C.CO2的平衡转化率为25%
D.该温度时化学平衡常数为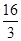 (mol/L)-2
(mol/L)-2
②在相同温度、相同容积的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
|
容器 |
容器1 |
容器2 |
容器3 |
|
反应物投入量(始态) |
1molCO2、3molH2 |
0.5molCO2、1.5molH2 |
1molCH3OH、1molH2O |
|
CH3OH的平衡浓度/mol•L-1 |
c1 |
c2 |
c3 |
|
平衡时体系压强/Pa |
p1 |
p2 |
p3 |
则下列各量的大小关系为c1___________c3,p2_________p3(填“大于”、“等于”或“小于”)。
(4)近年来,甲醇燃料电池技术获得了新的突破,如图所示为甲醇燃料电池的装置示意图。电池工作时,分别从b、c充入CH3OH、O2,回答下列问题:
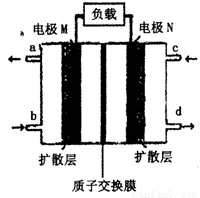
①从d处排出的物质是___________,溶液中的质子移向电极__________(填“M”或“N”);
②电极M上发生的电极反应式为__________________________。
(16分、每空2分)(1)CH4+H2O CO+3H2
CO+3H2
(2)CO(g)+2H2(g)=CH3OH(g) △H=(a-b)kJ/mol (3)①BD ②等于;小于
(4)①H2O N ②CH3OH+H2O-6e-=CO2↑+6H+
【解析】
试题分析:(1)反应物是甲烷和水,生成物是一氧化碳和氢气,根据原子生活借助于观察法配平,反应条件是高温和催化剂,所以该反应的化学方程式是CH4+H2O CO+3H2。
CO+3H2。
(2)根据根据图像可知,反应物的总能量高于生成物的总能量,因此反应是放热反应,其反应热△H=(a-b)kJ/mol,所以其热化学反应方程式为CO(g)+2H2(g)=CH3OH(g) △H=(a-b)kJ/mol。
(3)①A、根据图像可知,3min后各物质的浓度还发生变化,所以3min时该反应未达到平衡,故A错误; B、根据图像可知,在0~10min内甲醇的浓度增加了0.75mol/L,所以根据反应的化学方程式可知,消耗氢气的浓度是0.75mol/L×3=2.25mol/L,因此0~10min时用H2表示的反应速率=2.25mol/L÷10min=0.225mol/(L·min),故B正确;C、根据图像可知CO2的平衡转化率=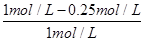 ×100%=75%,故C错误; D、根据图像和以上分析可知,平衡时c(CO2)=0.25mol/L,c(CH3OH)=c(H2O)=0.75mol/L,c(H2)=3c(CO2)=0.75mol/L,所以该温度下反应的化学平衡常数K=
×100%=75%,故C错误; D、根据图像和以上分析可知,平衡时c(CO2)=0.25mol/L,c(CH3OH)=c(H2O)=0.75mol/L,c(H2)=3c(CO2)=0.75mol/L,所以该温度下反应的化学平衡常数K=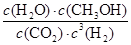 =
=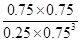 =
=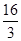 (mol/L)-2,D正确,答案选BD。
(mol/L)-2,D正确,答案选BD。
②根据方程式并采用一边倒的方法可知,1molCH3OH、1molH2O完全转化为反应物就是1molCO2、3molH2,因此容器1和容器3是等效平衡,所以平衡时甲醇的浓度c1等于c3;容器2相当于在容器1的基础上减小压强,平衡向逆反应方向移动,则平衡时p2 小于p3。
(4)①原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。因此该燃料电池中,负极通入甲醇,正极通入氧气。c电极上充入氧气,即电极N是正极,氧气得电子和氢离子反应生成水,所以d出来的是水,原电池放电时,氢离子向正极N极移动。
②电极M是负极,通入的是甲醇,失去电子发生氧化反应,因此发生的电极反应式为CH3OH+H2O-6e-=CO2↑+6H+。
考点:考查反应方程式、热化学反应方程式、电极反应式的书写;等效平衡的判断和应用;反应速率和平衡常数的计算以及电化学原理的应用等


科目:高中化学 来源: 题型:阅读理解
| ||
| ||
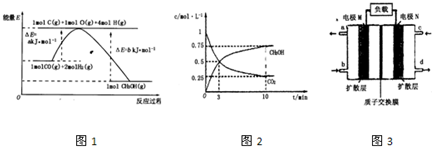
| 16 |
| 3 |
| 容器 | 容器1 | 容器2 | 容器3 |
| 反应物投入量(始态) | 1molCO2、3molH2 | 0.5molCO2、1.5molH2 | 1molCH3OH、1molH2O |
| CH3OH的平衡浓度/mol?L-1 | c1 | c2 | c3 |
| 平衡时体系压强/Pa | p1 | p2 | p3 |
查看答案和解析>>
科目:高中化学 来源: 题型:022
近年来,北京、成都等市率先在公交车和出租车中推行用天然气代替汽油作燃料的改革,取得了显著进展.走上街头你会发现不少公交车和出租车上印有“CNG”的标志,代表它们是以天然气作为燃料的汽车.试问:(1)成都市政府推广这一改革的主要目的是________(填字母).
(2)天然气是___________在隔绝空气的条件下,经微生物发酵作用而生成的,因此,天然气中贮藏的化学能最终来自于____________.
(3)天然气的主要成分是_________,该主要成分若出现于煤矿的坑道内,并达到一定浓度时遇____________,便会立即出现瓦斯爆炸.
(4)天然气的主要成分是一种很好的燃料.已知4 g该主要成分完全燃烧生成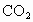 气体和液态
气体和液态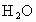 ,放出222.5kJ的热量,则上述成分燃烧的热化学方程式为__________.
,放出222.5kJ的热量,则上述成分燃烧的热化学方程式为__________.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
近年来,北京、成都等市率先在公交车和出租车中推行用天然气代替汽油作燃料的改革,取得了显著进展.走上街头你会发现不少公交车和出租车上印有“CNG”的标志,代表它们是以天然气作为燃料的汽车.试问:(1)成都市政府推广这一改革的主要目的是________(填字母).
(2)天然气是___________在隔绝空气的条件下,经微生物发酵作用而生成的,因此,天然气中贮藏的化学能最终来自于____________.
(3)天然气的主要成分是_________,该主要成分若出现于煤矿的坑道内,并达到一定浓度时遇____________,便会立即出现瓦斯爆炸.
(4)天然气的主要成分是一种很好的燃料.已知4 g该主要成分完全燃烧生成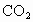 气体和液态
气体和液态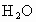 ,放出222.5kJ的热量,则上述成分燃烧的热化学方程式为__________.
,放出222.5kJ的热量,则上述成分燃烧的热化学方程式为__________.
查看答案和解析>>
科目:高中化学 来源:2013年山东省泰安市高考化学二模试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com