
【题目】在标准状况下,将22.4L HCl完全溶于1L水中(水的密度近似为1g/mL),溶液的密度为ρ g/cm3 , 溶液的体积为V mL,溶质的质量分数为w,溶质的物质的量浓度为c mol/L.下列叙述中正确的是( )
①w= ![]() ×100% c=1molL﹣1 向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w 所得溶液中含有NA个HCl分子.
×100% c=1molL﹣1 向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w 所得溶液中含有NA个HCl分子.
A.全部
B.①③④
C.①③
D.只有①
科目:高中化学 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为( )
A. 1:2:3 B. 1:6:9 C. 1:3:3 D. 1:3:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,导致浓度偏高的原因可能是 ( )
A. 移液时,不慎将液体流到瓶外 B. 容量瓶盛过NaOH溶液,使用前未洗涤
C. 容量瓶中原有少量的蒸馏水 D. 定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( ) 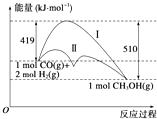
A.该反应的△H=+91 kJmol﹣1
B.加入催化剂,该反应的△H变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则△H减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)3Z(g),平衡时,X,Y,Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X,Y,Z的体积分数不变.下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是
①过滤、②蒸发、③溶解、④向容量瓶转移液体。
A.①和④B.①和③C.③和④D.①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。
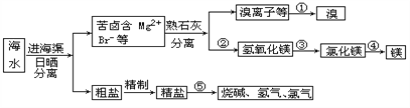
请回答下列问题:
(1)①步主要反应的的离子方程式:_____________________________________________。
(2)分离出氢氧化镁的操作为________________________________,
第③步需要加入________________________________________。
(3)将粗食盐中含有的Mg2+、Ca2+和SO42—等杂质除去,加入的试剂有(按加入顺序填入_________________(只要求填一组合理的答案即可) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含碳的化合物能形成上千万种化合物,并且有的物质之间很容易发生转化.请回答下列问题:
(1)有机物M在有光的时候很容易转化成N,其过程如图: 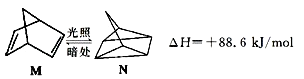
其中较稳定的物质是M,原因是 .
(2)已知 ![]() (l)的燃烧热为3267.5kJmol﹣1 ,
(l)的燃烧热为3267.5kJmol﹣1 , ![]() (l)+6O2(g)═6CO2(g)+3H2(g)
(l)+6O2(g)═6CO2(g)+3H2(g)
△H=a kJmol﹣1 , 则a﹣3267.5(填“>”、“<”或“=”).
(3)使Br2(g)和H2O(g)在1500℃时与焦炭反应,生成HBr和CO2 , 当有1mol Br2(g)参与反应时释放出125kJ热量,写出该反应的热化学方程式 .
(4)将C(石墨)、Al粉和TiO2固体在一定比例的条件下,在极高的温度下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=﹣1440kJmol﹣1 , 则反应过程中,每转移amol电子放出的热量为(用含a的表达式表示).
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=+490.0kJmol﹣1
CO(g)+ ![]() O2(g)=CO2(g)△H=﹣280.0kJmol﹣1
O2(g)=CO2(g)△H=﹣280.0kJmol﹣1
C(石墨)+O2(g)=CO2(g)△H=﹣390.5kJmol﹣1
2Fe2O3(s)=4Fe(s)+3O2(g)△H= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com