
【题目】草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O4—、C2O42—,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
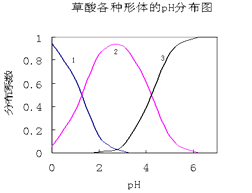
(1)图中曲线1表示________________的分布系数变化。
(2)现有物质的量浓度均为0.1mol/L的下列溶液:
a. Na2C2O4 b. NaHC2O4 c. H2C2O4 d. (NH4)2C2O4 e. NH4HC2O4
已知NaHC2O4溶液显酸性。
①NH4HC2O4显_____性(填“酸”、“碱”或“中”)
②Na2C2O4溶液中,![]() ____2 (填“>”、“=”、“<”), 原因是______________________________________________(用离子方程式表示)。
____2 (填“>”、“=”、“<”), 原因是______________________________________________(用离子方程式表示)。
③常温下,向10 mL 0. 1 mol/L H2C2O4溶液中滴加0.1 mol/L NaOH溶液,随着NaOH溶液体积的增加,当溶液中c(Na+)=2c(C2O42-)+c(HC2O4-)时,溶液显_______性(填“酸”、“碱”或“中”),且V(NaOH)______10 mL(填“>”、“=”或“<”)。
④五种溶液中c(H2C2O4)由大到小排列的顺序是 ________________________________。
【答案】 H2C2O4 酸 > C2O42-+H2O![]() HC2O4-+OH- 中 > c > e > b > d > a
HC2O4-+OH- 中 > c > e > b > d > a
【解析】(1). 因草酸的浓度越大,溶液的pH越小,根据图象可知,曲线1随pH的增大而逐渐降低,所以曲线1为草酸,故答案为:H2C2O4;
(2). ①. 因NaHC2O4溶液显酸性,说明HC2O4-的电离程度大于水解程度,因铵根离子水解也会使溶液显酸性,所以NH4HC2O4溶液显酸性,故答案为:酸;
②. 草酸钠中的草酸根离子是弱酸阴离子,可以发生水解反应C2O42-+H2O![]() HC2O4-+OH-,所以草酸钠溶液中
HC2O4-+OH-,所以草酸钠溶液中![]() >2,故答案为:>;C2O42-+H2O
>2,故答案为:>;C2O42-+H2O![]() HC2O4-+OH-;
HC2O4-+OH-;
③. 根据电荷守恒可知:c(Na+)+c(H+)=2c(C2O42-)+c(HC2O4-)+c(OH-),当溶液中c(Na+)=2c(C2O42-)+c(HC2O4-)时,c(H+)=c(OH-),所以溶液呈中性;草酸氢钠溶液呈酸性,要使溶液呈中性,则氢氧化钠溶液应稍微过量,所以V(NaOH)>10mL,故答案为:中;>;
④. 草酸根离子水解程度大于草酸氢根离子、铵根离子促进草酸根离子或草酸氢根离子水解,草酸电离程度较小,所以溶液中c(H2C2O4)由大到小排列的顺序是c>e>b>d>a,故答案为:c>e>b>d>a。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 ![]() 2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示. 
乙酸乙酯的实验室和工业制法常采用如图2装置:回答下列问题:
(1)写出A的电子式 .
(2)B、D分子中的官能团名称分别、 .
(3)写出下列反应的反应类型:①② , ④ .
(4)写出下列反应的化学方程式:①②④
(5)制取乙酸乙酯浓H2SO4的作用是:① , ② . 欲提高乙酸的转化率,可采取的措施有、等.
(6)碳酸钠溶液的作用是 , 导气管不能插入液面以下,原因是 . 加热前,大试管中加入几粒碎瓷片的作用是 .
(7)实验室可用乙醇来制取乙烯,将生成的乙烯通入溴的四氯化碳溶液,反应后生成物的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是
A. 用胆矾炼铜 B. 用铁矿石炼铁 C. 烧结粘土制陶瓷 D. 打磨磁石制指南针
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放上蒸发皿②加热搅拌③放置酒精灯④固定铁圈的位置⑤停止加热、余热蒸干。其正确的操作顺序是( )
A. ①②③④⑤B. ③④①②⑤C. ②③①④⑤D. ②①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠是实验室中常用的分析试剂,也常用于医疗和照相业。工业上用铁屑还原法制备NaI,其主要流程如下图,请回答下列问题:

(1)试写出铁屑转化为Fe(OH)3的离子反应方程式:______________________________________。
(2)判断碘是否已完全反应的实验方法是______________________________________________。
(3)分离出NaI样品需在低温无氧环境中进行,其目的是__________________________________。
(4)测定产品中NaI含量的方法是:______________
a.称取3.000 g样品、溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用0.1000 mol/LAgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19.00 mL。
①上述测定过程所需仪器中,需要检查是否漏液的仪器有______________________________。
②上述样品中NaI的质量分数为__________________________。
(5)已知Ksp(AgI)=1.5×10-16,将AgNO3和NaI的溶液混合,假设混合液中AgNO3的浓度为0.01 mol/L,则开始生成AgI沉淀时,混合液中c( I- )=____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解CuSO4溶液。若阳极上产生气体的物质的量为0.010 0 mol,则阴极上析出Cu的质量为 ( )
A.0.64 g
B.1.28 g
C.2.56 g
D.5.12 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氯气的叙述中,下列正确的是( )
A.氯气是一种黄绿色、有毒的气体
B.氯气可以与铁反应生成FeCl2
C.氯气不能溶解于水,所以可用排水法收集氯气
D.氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 
(1)若X极电极材料为铁,Y极电极材料为惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是 .
②该装置的总反应方程式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 , Y电极的材料是 ,
②Y电极的电极反应式 . (说明:杂质发生的电极反应不必写出)
(3)若X极材料为光滑的铁钉(已经处理),Y极的材料为锌,电解质溶液a为ZnCl2 , ①X极的电极反应式为
②Y极的电极反应式为
③电解质溶液a的浓度将(填“增大”、“减少”、“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为北京奥运会的奖牌﹣﹣“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )
A.Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO5MgO8SiO2H2O
B.从分类的角度看,Ca2Mg5Si8O22(OH)2为氧化物
C.玉石材料性质稳定,耐强酸和强碱的腐蚀
D.Ca2Mg5Si8O22(OH)2易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com