
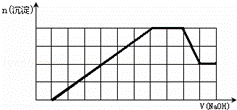
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、CO32﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()
A. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B. 原溶液中一定含有SO42﹣和Na+
C. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D. 反应最后形成的溶液中含有的溶质为Na2SO4
考点: 常见阳离子的检验;常见阴离子的检验.
专题: 图示题;压轴题;离子反应专题.
分析: A、根据生成沉淀的物质的量随NaOH溶液的体积变化的图象来确定存在的离子;
B、根据电荷守恒结合A选项的内容来确定存在的离子;
C、根据消耗氢氧化钠的量和生成沉淀的量来确定离子的物质的量的多少;
D、根据溶液中离子之间的反应来确定含有的溶质.
解答: 解:A、根据图象第一段,沉淀不是马上出现,可知一定有氢离子,酸碱中和反应是一切反应的优先反应,生成沉淀在后面溶解一部分,一定有铝离子,根据第三段,和氢氧化钠反应的离子不产生沉淀,证明是铵根离子,根据坐标得生成沉淀用了6体积的氢氧化钠,其中氢氧化铝溶解用了一体积的氢氧化钠,所以形成氢氧化铝用了三体积的氢氧化钠,还有三体积的氢氧化钠一定是被三价铁离子消耗,所以一定含有三价铁离子,一定不含碳酸根离子和镁离子,即原溶液中含有的阳离子是H+、NH4+、Fe3+、Al3+,故A错误;
B、根据A的推断,解题图象第二段和最后剩余沉淀的量,可以知道氢氧化铝的沉淀量和另一沉淀的量是相等的,即一定是三价铁离子,一定不含有镁离子,所以含有的阳离子是H+、NH4+、Fe3+、Al3+,一定不含碳酸根离子,溶液中需要正、负离子,故一定有阴离子SO42﹣,不能确定钠离子是否存在,故B错误;
C、根据坐标得生成沉淀用了6体积的氢氧化钠,其中氢氧化铝溶解用了1体积的氢氧化钠,所以形成氢氧化铝用了3体积的氢氧化钠,还有3体积的氢氧化钠一定是被三价铁离子消耗,原溶液中含有的Fe3+和Al3+的物质的量之比为1:1,故C正确;
D、加入NaOH溶液,钠离子实际不参加反应,则反应后溶液中钠离子一定存在,所以最后溶液中含有的溶质不一定为Na2SO4,故D错误.
故选C.
点评: 本题是一道有关离子检验的综合知识题目,考查角度很广,难度较大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
在日常生活中,与化学反应速度有关的做法是( )
|
| A. | 用热水溶解蔗糖以加速溶解 |
|
| B. | 把块状煤碾成粉末状再燃烧 |
|
| C. | 真空包装食品,以延长保质期 |
|
| D. | 低温冷藏使食品延缓变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将等质量的锌粒(wg)分别投入VL pH=2的盐酸和醋酸(含醋酸n mol),结果发现一种溶液中Zn有剩余,有关叙述正确的是( )
|
| A. | 0.325V<w<32.5n |
|
| B. | 产生H2的平均反应速率盐酸大于醋酸 |
|
| C. | 产生H2的量盐酸多于醋酸 |
|
| D. | 与醋酸反应时锌有剩余 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是()
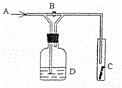
A. 浓H2SO4 B. 饱和Na2CO3溶液
C. 浓NaOH溶液 D. 饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
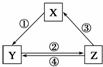
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是()
选项 X Y Z 箭头上所标数字的反应条件
A CaO Ca(OH)2 CaCO3 ①常温遇水
B AlCl3 NaAlO2 Al(OH)3 ②通入CO2
C Na2CO3 NaOH NaHCO3 ④过量Ca(OH)2溶液
D Cl2 Ca(ClO)2 HClO ③加浓盐酸
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
如图中每一方格表示有关的一种反应物或生成物.A、C为无色气体.

(1)物质M可以是 或 ,C是 ,F是 .
(2)反应①的化学方程式 .
(3)反应②的离子方程式 .
(4)F→G的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
1﹣丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )
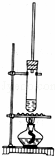
|
| A. | 不能用水浴加热 |
|
| B. | 长玻璃管有冷凝回流作用 |
|
| C. | 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
|
| D. | 加入过量乙酸可以提高1﹣丁醇的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为了比较①H﹣OH,②CH3COOH,③CH3CH2﹣OH,④H2CO3,⑤苯酚五种物质分子中﹣OH上氢原子的活动性顺序,某课外活动小组设计了如下表所示的实验方案.请你利用有关实验仪器及给出的试剂,填写表中的空格,完成上述实验方案.可供选用的试剂有:紫色石蕊试液、金属钠、氢氧化钠溶液、碳酸钠溶液.实验中所需仪器自选.
| 实验步骤和操作 | 实验现象 | 结论(﹣OH上氢原子活动性顺序) |
| (1)五种物质各取少量于五支试管中,各加入紫色石蕊试液2~3滴 | ②④变红,其它不变 | ②、④>①、③、⑤ |
| (2) | ||
| (3)①、③、⑤各取少量于试管中,各加入少量NaOH溶液 | ⑤由浑浊变澄清 | ⑤>①、③ |
| (4) |
(5)通过以上实验比较,从而得出这五种物质分子中﹣OH上氢原子的活动性由强到弱的顺序为 (填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的KHSO4溶液。当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与KHSO4溶液的体积之和,则Ba(OH)2溶液与KHSO4溶液的体积比是( )
A.1∶9 B.1∶1 C.1∶2 D.1∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com