
| A. | NaOH | B. | NaCl | C. | H2SO4 | D. | NH4Cl |
分析 升高温度促进水的电离,水电离的氢离子浓度增大;升高温度后能够促进盐的水解,结合溶液的pH=-lgc(H+)及溶液中氢离子浓度变化分析溶液pH变化.
解答 解:A.氢氧化钠中氢离子由水电离,升高温度,水电离的氢离子浓度增大,所以氢氧化钠溶液的pH减小,故A错误;
B.氯化钠中氢离子由水电离,升高温度,水电离的氢离子浓度增大,所以pH减小,故B错误;
C.H2SO4中氢离子主要有酸电离,水电离的氢离子很少,所以升高温度对硫酸的电离没影响,所以溶液中的氢离子浓度基本不变,则pH基本不变,故C正确;
D.NH4Cl中氢离子由水电离,升高温度,促进盐的水解,溶液中氢离子浓度增大,所以pH减小,故D错误;
故选C.
点评 本题考查了温度对水的电离和盐的水解的影响,主要考查了溶液中氢离子浓度的变化,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,试题培养了学生的灵活应用能力.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 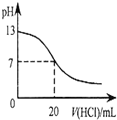 表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 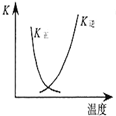 图中曲线表示反应2SO2(g)+O2(g)═2SO3(g)△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 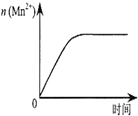 表示10 mL 0.01 mol•L-1 KMnO4酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. |  图中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 萃取 | C. | 分液 | D. | 蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,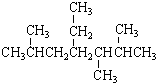 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 石油裂解可以得到氯乙烯,煤液化可得到焦炭、煤焦油、焦炉气等 | |
| D. | 1.0 molHC≡CCHO最多能与3.0 mol H2完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卢瑟福提出了带核的原子结构模型 | |
| B. | 已知PM2.5是指大气中直径≤2.5×10-6m的颗粒物,受PM2.5污染的大气不一定能产生丁达尔现象 | |
| C. | 借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有的非金属元素 | |
| D. | 并不是所有金属元素都可以用焰色反应来确定其存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NA个NH3分子气体溶于1L水中得到1mol•L-1的氨水 | |
| B. | 标况下,22.4L三氧化硫中含有NA个分子 | |
| C. | 1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子 | |
| D. | 各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中混有溴,加入四氯化碳后,用分液漏斗分液 | |
| B. | 乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液 | |
| C. | 乙烷中混有乙烯,加入氢气在一定条件下充分反应 | |
| D. | 苯甲醛中混有苯甲酸,加入生石灰,再加热蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com