
| 30 |
| 12 |
 +Br2
+Br2| 光照 |
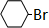 +HBr,
+HBr, +Br2
+Br2| 光照 |
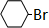 +HBr;
+HBr;| 一定条件 |
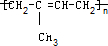 ,
,| 一定条件 |
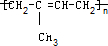 ;
;| 30 |
| 12 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、常温下金属均为固态 |
| B、合金的很多性能与组成它们的纯金属不同 |
| C、铁在潮湿的空气中比在干燥的空气中更易生锈 |
| D、铝在空气中表面会生成致密的氧化铝薄膜,使铝具有很好的抗腐蚀性能 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 在上述条件下发生反应,得到的最终产物结构式分别是:
在上述条件下发生反应,得到的最终产物结构式分别是: ,用Na、NaOH、NaHCO3与等物质的量的该有机物完全反应时,消耗Na、NaOH、NaHCO3的物质的量之比为
,用Na、NaOH、NaHCO3与等物质的量的该有机物完全反应时,消耗Na、NaOH、NaHCO3的物质的量之比为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 I.工业上用洗净的废铜屑作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是
I.工业上用洗净的废铜屑作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是| 空气 |
| △ |
| 浓硝酸 |
| 浓硫酸 |
| Ba(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2H4+O2═N2+2H2O△H=-534.4kJ/mol |
| B、N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-16.7kJ/mol |
| C、N2H4(g)+O2(g)═N2(g)+2H2O(l)△H=-534.4kJ/mol |
| D、N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com