
 合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.| A. | 升高温度 | B. | 分离出部分氨气 | C. | 降低压强 | D. | 增大反应物浓度 |
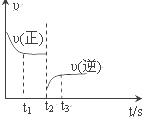
分析 该反应是一个反应前后气体体积减小的放热反应,根据图知,t1时建立平衡正逆反应速率相等,t2时改变某一条件,逆反应速率降低,随着反应进行逆反应速率增大,说明平衡正向移动,则改变条件时正反应速率大于逆反应速率,结合温度、压强、浓度对化学反应平衡移动影响分析解答.
解答 解:该反应是一个反应前后气体体积减小的放热反应,根据图知,t1时建立平衡正逆反应速率相等,t2时改变某一条件,逆反应速率降低,随着反应进行逆反应速率增大,说明平衡正向移动,则改变条件时正反应速率大于逆反应速率,
A.如果升高温度,正逆反应速率都增大,则改变条件时逆反应速率应该在原来平衡速率上方,与图象不符合,故A错误;
B.分离出部分氨气,生成物浓度降低,则逆反应速率降低,平衡正向移动,所以正反应速率大于逆反应速率,符合图象,故B正确;
C.减小压强,正逆反应速率都减小,但正反应速率减小程度大于逆反应速率减小程度,反应向逆反应方向移动,与图象不符合,故C错误;
D.增大反应物浓度,改变条件瞬间,逆反应速率不变,与原来平衡点有接触点,与图象不符合,故D错误;
故选B.
点评 本题以图象分析为载体考查外界条件对反应速率、化学平衡的影响,明确图中纵横坐标含义及曲线变化趋势含义是解本题关键,侧重考查学生分析判断能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 在101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ热量,H2的燃烧热为-285.8kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度 | |
| C. | 在101k Pa时,1mol C与适量O2 反应生成1mol CO时,放出110.5kJ热量,则C的燃烧热为110.5kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l),△H=-57.31 kJ•mol-1.若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
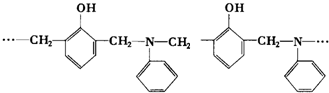
| A. | 2种,取代和加聚反应 | B. | 2种,加成和缩聚反应 | ||
| C. | 3种,取代和加聚反应 | D. | 3种,加成和缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,4υ正(O2)=5υ逆(NO ) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 恒温、恒容时,当混合气体的密度不再变化时,表示反应达到了化学平衡状态 | |
| D. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:H2Y<HZ | B. | 原子半径:W>X>Z>Y | ||
| C. | 离子半径:W2+>Y2- | D. | 碱性:XOH<W(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(Na+)>c(CH3COO-) | B. | c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | ||
| C. | c(Na+)<c(CH3COO-) | D. | c(Na+)<c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 单位电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com