

| A. | ⑦⑧ | B. | ⑤⑦ | C. | ①②③ | D. | ④⑥⑧ |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同,研究对象是有机物,注意如果含有官能团,则官能团的种类及数目必须完全相同.
解答 解:A.⑧为2-甲基-1-丙烯,为单烯烃,⑦为1,3-戊二烯,是二烯烃,分子结构不相似,所以⑦⑧一定不属于同系物,故A错误;
B.⑤为1,3-丁二烯,⑦为1,3-戊二烯,二者都是二烯烃,分子结构相似,分子间相差1个CH2原子团,所以⑤⑦一定属于同系物,故B正确;
C.①为甲苯,②为萘,③为苯乙烯,苯乙烯分子中含有苯环和碳碳双键,萘中含有2个苯环,三者结构不同,一定不属于同系物,故C错误;
D.④为乙烯,分子中含有碳碳双键,⑥为丙烯或者环丙烷,而⑧为2-甲基-1-丙烯,三者结构不一定相似,所以④⑥⑧不一定互为同系物,故D错误;
故选B.
点评 本题考查了同系物的判断,题目难度不大,注意掌握常见有机物结构与性质,明确同系物的概念及判断方法,特别注意互为同系物的有机物,如果含有官能团时,官能团的类型及数目必须相同.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
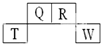 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )| A. | H2R2的分子中既含有极性共价键,又含有非极性共价键 | |
| B. | T的氧化物是一种良好的半导体材料 | |
| C. | Q、R的简单氢化物分子所含质子数、电子数与Ne分子相同 | |
| D. | Q的氢化物与W的氢化物反应有白烟现象,且生成物中既含有离子键,又含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
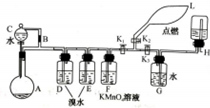 有一同学准备用Al4C3(含少量Mg2C3杂质)制取某种气种X(其装置图如图所示,夹持装置略),并进行以下实验项目:
有一同学准备用Al4C3(含少量Mg2C3杂质)制取某种气种X(其装置图如图所示,夹持装置略),并进行以下实验项目:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ( CH3)2CH( CH2)2 CH3 | B. | CH3 CH2 CH( CH3) CH2 CH3 | ||
| C. | ( CH3)2CHCH2CH( CH3)2 | D. | ( CH3)3 C CH2 CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应 | |
| B. | 等质量锌粒和锌粉分别与等量1 mol/L HCl反应 | |
| C. | 等体积等浓度HCl和CH3COOH分别与等质量的Na2CO3粉末反应 | |
| D. | 等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
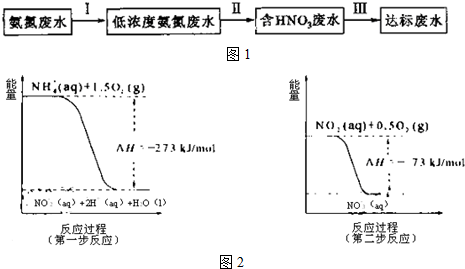
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/L | 0.0 | 9.9 | 17.2 | V=? |
| A. | 0~2min H2O2平均反应速率比4~6min慢 | |
| B. | 反应至6min时,共产生O244.8L | |
| C. | 0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol•L-1•min-1 | |
| D. | 反应至6min时,c(H2O2)=0.3mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com