
| 实验序号 | 实验操作 | 现象 | 反应的可能情况 |
| ① | 滴加少量淀粉碘化钾溶液,振荡 | III | |
| ② | 滴加少量棕红色的KI3溶液,振荡 | II | |
| ③ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液呈紫色 | |
| ④ | 加入几小块CaCO3固体 | 有气泡产生 |
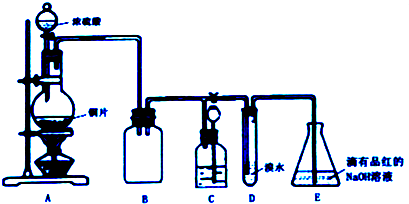
分析 由图可知,A中发生Cu与浓硫酸的反应生成二氧化硫,B作安全瓶,可防止倒吸,D中发生SO2+Br2+2H2O=H2SO4+2HBr,E中NaOH溶液吸收尾气,
(1)A中发生Cu与浓硫酸的反应生成二氧化硫,B仪器可防止倒吸;
(2)利用二氧化硫与溴水溶液的反应来分析;
(3)装置C的作用是贮存多余的气体,所以C中应放置的液体不能与二氧化硫反应,也不能溶解二氧化硫,据此分析;
(4)利用稀硫酸的性质来分析;
(5)①次氯酸可氧化KI;
②SO2氧化I-使溶液褪色;
③HSO3-与高锰酸钾可发生氧化还原反应;
④加入几小块CaCO3固体,生成CO2气体,溶液显酸性;
(6)电离显酸性,水解显碱性,则测定pH即可.
解答 解:(1)浓硫酸和铜反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;B装置的锥形瓶是空的,可以防止倒吸;故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;防止C中液体倒吸入A中(或防倒吸,或安全瓶);
(2)溴水具有氧化性,二氧化硫具有还原性,二者发生氧化还原反应;D中NaOH全部转化为NaHSO3,再通入SO2,品红会褪色;故答案为:还原;溶液红色褪去;
(3)装置C的作用是贮存多余的气体,所以C中应放置的液体不能与二氧化硫反应,也不能溶解二氧化硫,所以应为饱和NaHSO3溶液,故答案为:饱和NaHSO3溶液;
(4)某同学认为H2SO4也有剩余,则可以检验H+或测定稀硫酸的pH确定稀硫酸的存在;故答案为:b c;
(5)①如果你漂白粉过量,发生反应NaHSO3+Ca(ClO)2═CaSO4↓+NaCl+HClO,次氯酸氧化碘离子为碘单质,碘遇淀粉变蓝,溶液变为蓝色;②如果你漂白粉不足,发生反应4NaHSO3+Ca(ClO)2+CaCl2═2CaSO4↓+4NaCl+2SO2↑+2H2O,SO2氧化I-使溶液褪色;③如果HSO3-与ClO-刚好反应完,方程式为2NaHSO3+Ca(ClO)2+CaCl2═2CaSO4↓+2NaCl+2HCl,滴入加少量酸性KMnO4溶液,溶液显紫色,说明没有还原性物质,反应可能是Ⅰ或Ⅲ;④加入几小块CaCO3固体,生成CO2气体,溶液显酸性,可能是Ⅰ或Ⅱ;
故答案为:
| 实验序号 | 实验操作 | 现象 | 反应的可能情况 |
| ① | 滴加少量淀粉碘化钾溶液,振荡 | 溶液变为蓝色 | III |
| ② | 滴加少量棕红色的KI3溶液,振荡 | 溶液褪色 | II |
| ③ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液呈紫色 | Ⅰ或Ⅲ |
| ④ | 加入几小块CaCO3固体 | 有气泡产生 | Ⅰ或Ⅱ |
点评 本题考查制备实验方案的设计,为高频考点,把握制备实验装置、原理、物质的性质及反应为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 二氧化碳与石灰水:CO2+OH-=HCO3- | |
| B. | 氯化铁和硫氢化钠:2Fe3++2HS-=Fe2++2H++FeS↓+S↓ | |
| C. | 硫酸亚铁铵和氢氧化钡:2NH4++2OH-+Ba2++SO42-=2NH3•H2O+BaSO4↓ | |
| D. | 在酸性条件下亚硫酸钠和硫化钠:2SO32-+2S2-+8H+=3S↓+SO2↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
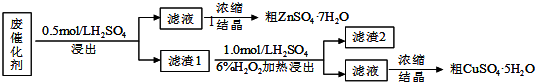
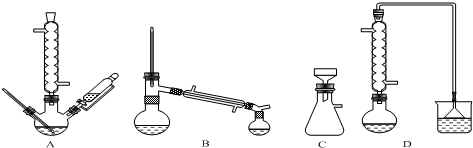
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
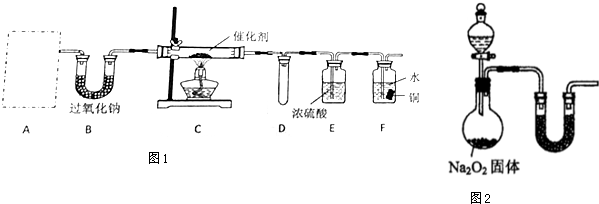
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com