
在一定条件下,RO3n-与氟气可发生如下反应: RO3n—+ F2 + 2OH- = RO4—+ 2F- + H2O
从而可知在RO3n-中,元素R的化合价是( )
A、+4 B、+5 C、+6 D、+7
科目:高中化学 来源: 题型:
重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下:

试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有 。铁在周期表的位置是 。
(2)操作Ⅱ的名称是 。
(3)固体X的主要成分是___________,沉淀Y的主要成分是 。
(4)流程中①酸化所用的酸和②钾盐Z最合适的是(填符号)________,
A.盐酸和氯化钾 B.硫酸和氯化钾 C.硫酸和硫酸钾 D.次氯酸和次氯酸钾
酸化反应的离子方程式为 。
(5)FeO·Cr2O3与氯酸钾、氢氧化钠高温反应化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列说法正确的是 ( )

A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.图中所涉及的盐类物质均可发生水解
D.NH3和NO2在一定条件下可以发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(l)+3O2(g)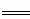 2CO2(g)+4H2O(g)
2CO2(g)+4H2O(g) 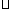 H1=-1275.6kJ·mol-1
H1=-1275.6kJ·mol-1
②2CO(g)+O2(g)  2CO2(g)
2CO2(g) 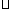 H2=-566.0kJ·mol-1
H2=-566.0kJ·mol-1
③H2O(g)=H2 O(l)
O(l) 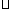 H3=-44.0kJ·mol-1
H3=-44.0kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式 。
(2)生产甲醇的原料CO和H2来源于下列反应:
CH4(g)+H2O(g) CO(g)+3H2(g)
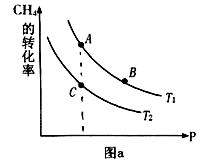
CO(g)+3H2(g) 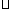 H>0
H>0
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则T1 T2(填“<”、“>”或“=",下同);A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为 ;
②100℃时,将1 mol CH4和2 mol H2O通入容积为1L的定容密闭容器中发生反应,能说明该反应已经达到平衡状态的是 (填序号)。
a.容器的压强恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 molH2
c.容器内气体密度恒定
d.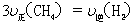
如果 达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K= 。
达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K= 。
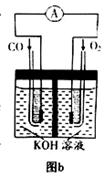
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:

去。经检测发现滤液中仍含有一定量的SO42—,其原因是
。【已知:Ksp(BaSO4)= 1.1 ×10—10 Ksp(BaCO3)= 5.1 ×10—9】
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有 (填化学式),发生器中生成ClO2的化学方程式为 。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 (D) +24NaClO3+12H2SO4=
(D) +24NaClO3+12H2SO4= ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+
(3)ClO2和Cl2均能将电镀废水中的CN—氧化为无毒的物质,自身被还原为Cl—。 处理含CN—相同时的电镀废水,所需Cl2的物质的量是ClO2的 倍
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)已知白磷和氯酸溶液可发生如下反应:
P4 + HClO3 + === HCl + H3PO4
配平并完成上述反应方程式,该反应的氧化剂是______________。
(2)白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:
11P4 + 60CuSO4 + 96H2O === 20Cu3P + 24 H3PO4 + 60 H2SO4
该反应的氧化产物是______________,若有1.1mol P4反应,则有________mol电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
由于用氯气对饮用水消毒,会使水中的有机物发生氯代,生成有机含氯化合物,于人体有害,世界环保联盟即将全面禁止这种消毒方法,建议采用广谱性具有强氧化性的高效消毒剂二氧化氯(ClO2).C102极易爆炸,生产和使用时尽量用稀有气体稀释,避免光照、震动或加热.
(1)在C102分子中,氯元素的化合价
(2)欧洲一些国家用NaClO3氧化浓盐酸来制 C102,同时有Cl2生成,且Cl2的体积为ClO2体积的一半,表示这一反应的化学方程式是 。
(3)我国广泛采用将经干燥空气稀释的氯气,通入有固体亚氯酸钠(NaClO2)的柱内制得C102,这一反应的学方程式是 ,和欧洲的方法相比,我国这一方法的主要优点是 。
(4)在酸性溶液中,用草酸钠(Na2C204)还原NaClO3也可制得C102,表示这一反应的离子方程式是 ,此法的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中可以提取溴,主要反 2Br-+Cl2=Br2+2C1-.下列说法正确的是 ( )
A.溴离子具有氧化性 B.氯气是还原剂
C.该反应属于复分解反应 D.氯气的氧化性比溴单质强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中正确的是( )
A.实验室用烧碱溶液除去尾气中的Cl2:Cl2+OH-====Cl-+HClO
B.向AlCl3溶液中滴加过量氨水制备Al(OH)3:
Al3++3NH3·H2O====Al(OH)3↓+3NH4+
C.用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.用FeCl3溶液腐蚀铜制印刷电路板:Fe3+ +Cu====Fe2++Cu2+
+Cu====Fe2++Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com