
【题目】下列说法正确的是
A. 若H2O2分解产生1molO2,理论上转移的电子数约为4×6.02×1023
B. 室温下,pH=3的CH3COOH溶液与 pH=11的NaOH溶液等体积混合,溶液pH>7
C. 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
D. 一定条件下反应N2+3H2![]() 2NH3达到平衡时,3v正(H2)=2v逆(NH3)
2NH3达到平衡时,3v正(H2)=2v逆(NH3)
【答案】C
【解析】
A. H2O2分解产生1molO2,反应中O元素化合价由-1价升高到0价,转移2mol电子,因此转移的电子数目为2×6.02×1023,A错误;
B. 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,由于醋酸是弱酸,在溶液中存在电离平衡,醋酸浓度大于NaOH浓度,醋酸过量,溶液pH<7,B错误;
C.钢铁水闸可用牺牲阳极的阴极保护方法或外加电流的阴极保护法防止其腐蚀,C正确;
D.一定条件下反应N2+3H2![]() 2NH3反应,速率关系符合系数比,即v正(H2):v正(NH3)=3:2,当反应达到平衡时,v正(NH3)=v逆(NH3),则达到平衡时,应为2v正(H2)=3v逆(NH3),D错误;
2NH3反应,速率关系符合系数比,即v正(H2):v正(NH3)=3:2,当反应达到平衡时,v正(NH3)=v逆(NH3),则达到平衡时,应为2v正(H2)=3v逆(NH3),D错误;
故合理选项是C。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次递增,X、Y、Z三种元素的原子序数之和为25,且Z和X的原子序数之和比Y的原子序数的2倍还多1,X原子核外有2个电子层,最外层电子数是核外电子数的2/3;W在所在周期中原子半径最小。回答下列问题:
(1)W在元素周期表中的位置是________________
(2)X的原子结构示意图是___________。
(3)用电子式表示Z2Y的形成过程:____________________。
(4)在Z2XY3溶液中加入足量MgCl2溶液,过滤沉淀,取滤液,再滴加CaCl2溶液,溶液仍然出现白色沉淀,说明Z2XY3与MgCl2的反应存在___________,该反应的离子方程式为__________。
(5)以X的简单氢化物、Y的单质为两电极原料,Z2Y溶于水形成的溶液为电解质溶液,可制备燃料电池。该燃料电池的负极反应为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
(1)分别写出三只烧杯中形成分散系的名称:
A________,B________,C________。
(2)写出C中形成分散系的化学方程式:_____________________________________。
(3)若不用化学试剂鉴别,写出鉴别B、C分散系的两种简单方法:
①______________________________________________________,
②________________________________________________________。
(4)向C中逐滴加入稀H2SO4,现象为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是

A. 离子半径: X>Y>Z
B. WX3和水反应形成的化合物是离子化合物
C. 最高价氧化物对应的水化物酸性:R>W
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置(图中夹持仪器略去)测定牙膏样品中碳酸钙的质量分数,下列说法错误的是
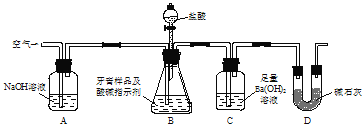
A.实验过程中持续通入空气可起到搅拌B、C中的反应物的作用
B.实验过程中滴加盐酸的速率不宜过快
C.依据装置C在反应前后的质量差测定的结果会偏高
D.C中的沉淀经过滤、干燥、称重后可确定牙膏样品中碳酸钙的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据信息填空:
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生反应2FeCl3 +Cu ===2FeCl2 +CuCl2,若将此反应设计成原电池,则负极所用的电极材料为____;当线路中转移0.2mol电子时,则被腐蚀的铜的质量为____。
(2)如图所示,把试管放入盛有25℃的饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中,可观察到溶液变浑浊,试回答下列问题:
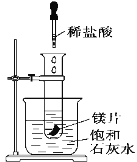
①产生上述现象的原因是___________________________;
②写出有关反应的离子方程式___________________。
③由实验推知,MgCl2和H2的总能量__________(填“大于”、“小于”或“等于”)Mg和HCl的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前科学家对化学键的研究已日趋完善,下列观点中正确的是( )
A.极性键和非极性键不能共存于同一物质中
B.单质分子中一定含有非极性共价键
C.离子化合物中一定含有离子键,可能含有极性键
D.金属元素和非金属元素之间形成的化学键均为离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于恒容密闭容器中进行的可逆反应2NO2(g)![]() 2NO(g)+O2(g),下列说法中能说明反应一定已经达到化学平衡状态的是( )
2NO(g)+O2(g),下列说法中能说明反应一定已经达到化学平衡状态的是( )
①单位时间生成n mol O2的同时生成2n mol NO2;
②2v正(NO2)=v逆(O2)
③NO2、NO、O2的物质的量浓度之比为2:2:1;
④容器内压强不再改变
⑤密闭容器中混合气体的密度不再改变;
⑥混合气体的平均相对分子质量不再改变
A.①④⑥B.②③⑤C.①②⑥D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com