
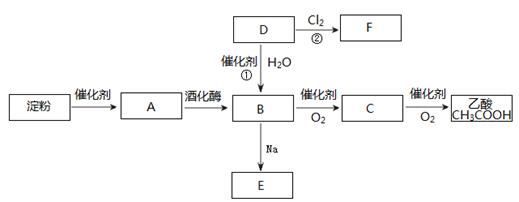
(1)写出C的结构简式 。
(2)反应①类型是 ,已知F的结构中无双键,则F的结构简式为 。
(3)写出B和乙酸发生酯化的化学方程式 。
(4)糖类、油脂、蛋白质均为人类重要的营养物质,下列说法正确的是: 。
A.化合物A与银氨溶液混合后,水浴加热生成银镜,说明A中存在醛基 |
B.油脂是高级脂肪酸和甘油形成的酯类高分子化合物,氨基酸分子中都存在氨基和羧基两种官能团 |
C.将绿豆大小的钠块投入B中,钠块浮于液面上,并有大量气泡产生 |
D.乙酸乙酯制备实验中用饱和碳酸钠溶液收集产物,乙酸乙酯在下层 |
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2017届陕西省西安市高三模拟(一)理综化学试卷(解析版) 题型:简答题
研究发现:一节电池烂在地里,能够使一平方米的土地失去利用价值。废旧电池的危害上要集中在其中所含的少量重金属上。将废旧锌锰电池回收处理,既能减少它对环境的污染,又能实现废电池的资源化利用。
(1)回收填料中的二氧化锰和氯化铵。已知:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。回收物质的流程如图所示。
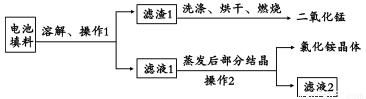
① 操作中先将电池填料研碎的目的是:________________。
② 操作l和操作2的名称都是___________,该操作中玻璃棒的作用是___________。
③ 灼烧滤渣l的目的是______________________。
(2)回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
①写出MnOOH与浓盐酸反应的化学方程式:________________。
② 锰回收新方法:向废旧锌锰电池内的混合物[主要成分MnOOH、Zn(OH)2]中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的化学方程式______________。与使用浓盐酸回收锰相比,新方法的优点是___________(答l点即可)。
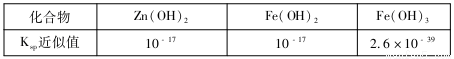
(3)用废电池的锌皮可用于回收制作ZnSO4·7H2O。过程中,需除去锌皮中的少量杂质铁,其方法是:常温下,加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中c(Fe3+)=_________。继续加碱调节pH为____时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。部分难溶的电解质溶度积常数(Ksp)如下表:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷(解析版) 题型:推断题
有关物质的转化关系如下图所示(部分物质和条件己略去)。A是由两种元素组成的难溶于水的物质,摩尔质量为88 g·mol-l;B是常见的强酸;C是一种气态氢化物;气体E能使带火星的木条复燃;F是最常见的无色液体;无色气体G能使品红溶液褪色;向含有I的溶液中滴加KSCN试剂,溶液出现血红色。请回答下列问题:
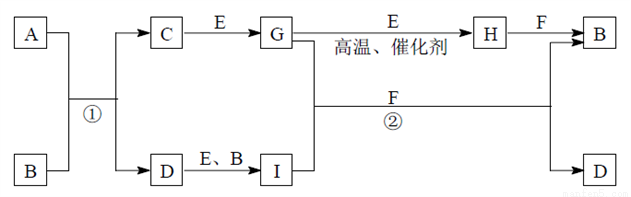
(1)G的化学式为_________________________。
(2)C的电子式为________________________。
(3)写出反应①的离子方程式:_____________________。
(4)写出反应②的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷(解析版) 题型:选择题
过氧乙酸(CH3COOOH)的制备反应为:CH3COOH +H2O2 CH3COOOH+H2O,下列有关该反应的说法正确的是
CH3COOOH+H2O,下列有关该反应的说法正确的是
A. 当消耗CH3COOH的速率与消耗H2O2的速率相等时,反应达到限度
B. 达反应限度时,CH3COOH、H2O2、CH3COOOH的浓度均不再变化
C. 达反应限度时,CH3COOH不再与H2O2发生反应
D. 若在反应中适当降低CH3COOH浓度,可提高反应速率
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷(解析版) 题型:选择题
国际纯粹与应用化学联合会(IUPAC)于2016年正式决定将113号新元素符号确定为Nh,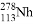 是它的一种核素。下列关于
是它的一种核素。下列关于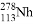 的说法正确的是
的说法正确的是
A. 质量数为113 B. 质子数为113 C. 相对原子质量为113 D. 中子数为113
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是
A. 铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B. 往溶液中滴入无色KSCN溶液,显红色
C. Fe2+和Fe3+物质的量之比为5∶1
D. 氧化产物和还原产物的物质的量之比为2∶5
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
下列变化需克服相同类型作用力的是 ( )
A. 碘和干冰的升华 B. 硅和C60的熔化
C. 氯化氢和氯化钠的溶解 D. 溴和汞的气化
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期周练(2)化学试卷(解析版) 题型:实验题
已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈—1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
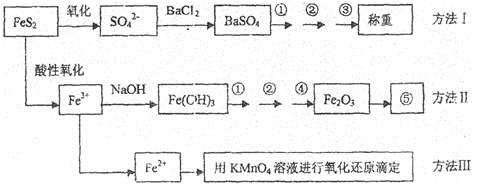
请同答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________、②___________、③________。
操作④、⑤用到的主要仪器是:④_________、⑤__________(每空填1~2个仪器)。
(2)判断溶液中SO42-离子己沉淀完全的方法是______________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A.砝码生锈 | B.定容时俯视 |
C.称量时物质和砝码位置反了(需要游码) | D.容量瓶用待装液润 |
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省泰安市高三第一轮复习质量检测(一模)理科综合化学试卷(解析版) 题型:选择题
短周期主族元素W、X、Y、Z的原子序数依次增大。W、Z同族,Y、Z相邻,W、Y、Z三种元素原子的最外层电子数之和为11,X原子最外层电子数等于最内层电子数的一半。下列叙述正确的是
A. 原子半径:Y>Z
B. 金属活动性:X<Y
C. 最简单氢化物的热稳定性:Z>W
D. Y元素的氧化物不溶于X元素最高价氧化物对应水化物的水溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com