
| A、熔点:MgBr2>Cs>Na |
| B、微粒半径:Ca2+>C1->Mg2+ |
| C、碱性:KOH>Mg(OH)2>Al(OH)3 |
| D、氧化性:Cu2+>Fe3+>K+ |


 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
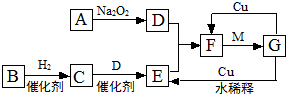
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯材料化学稳定性好,所以容易产生白色污染 |
| B、蚕丝制品和棉花制品可以通过灼烧的方法加以鉴别 |
| C、糖类、油脂、蛋白质一定条件下都能发生水解反应 |
| D、可用新制Cu(OH)2悬浊液检验尿液中是否含有葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
| B、H2O、CH3COOH、CaCO3均含有氧元素,都是氧化物 |
| C、HCl、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D、HNO3、浓硫酸都具有强氧化性,都是氧化性酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通入过量的SO2气体后:Ba2+、Mg2+、H+、Cl- | ||
| B、在滴加KSCN溶液呈红色的溶液中:Na+、NH4+、I-、SO42- | ||
C、常温下,在AG=lg[
| ||
| D、在饱和氨水中:Na+、Al3+、NO3-、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(OH-)=10-13mol?L-1的溶液中:Na+、NH4+、Cl-、NO3- |
| B、1.0 mol?L-1KI溶液中:Mg2+、Fe2+、SO42-、C1O- |
| C、c(Fe3+)=0.1 mol?L-1的溶液中:Na+、NH4+、HCO3-、SCN- |
| D、饱和氨水中:NH4+、Ag+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com