
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
���� ������ƽ�ⳣ�����¶ȱ仯�����¶ȶ�ƽ���ƶ���Ӱ�죬��Ӧ�Է����е��ж������ǡ�H-T��S��0���ݴ��жϣ�
����������ʽ�������������ʵ����仯����ƽ��ʱ�����ʵ���������ת���ʸ������CO��ת���ʣ�����Ũ�ȼ����ƽ�ⳣ�������ж��¶ȣ�
��� �⣺���ɱ����ݿ�֪���¶����ߣ�ƽ�ⳣ����С��˵��ƽ��������У����������ȷ�Ӧ��������ȷ�Ӧ������H1��0��CO��g��+2H2��g��?CH3OH��g����Ӧǰ�����������С���ر��S��0�������H-T��S��0��Ӧ�ڵ��������Է����У�
�ʴ�Ϊ���������£�
�ڰ���Ӧ��ַ�Ӧ�ﵽƽ����c��CO��=0.2mol/L�����ʵ���Ϊ0.4mol��
CO ��g��+2H2 ��g��?CH3OH ��g��
��ʼ����mol�� 2 6 0
�仯����mol�� 1.6 3.2 1.6
ƽ������mol�� 0.4 2.8 1.6
CO��ת����=$\frac{1.6mol}{2mol}$��100%=80%��
�ʴ�Ϊ��80%��
���� ���⿼���˻�ѧƽ���Ӱ�����غ��йؼ��㡢��Ӧ�Է����е��ж����ݵȣ��ѶȲ���ע������ƽ������Ӧ�ã�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �úϽ���۵�����ơ���֮�� | |
| B�� | �ƻ����γɵ��������Ϊ���������� | |
| C�� | �������ƺ����ֱ������������ᷴӦ�Ʋ���������� | |
| D�� | ���Ͻ���n��Na��=n��Al��������Ͷ�뵽������ˮ�У��ɵ���ɫ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
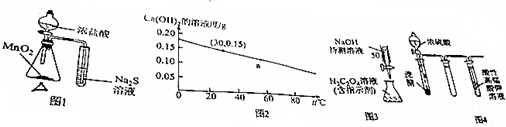
| A�� | ͼ1��װ�ÿ����ڱȽ�MnO2��Cl2��S�������� | |
| B�� | ͼ2��֪��30��ʱCa��OH��2��Һ��Ũ��һ������60��ʱ���¶� | |
| C�� | ͼ3��װ�ÿ�������֪Ũ�ȵ�H2C2O4��Һ�ⶨδ֪Ũ�ȵ�NaOH��Һ | |
| D�� | ͼ4��ʵ���������Ը��������Һ�������ݳ��֣�����Һ��ɫ��dz������ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

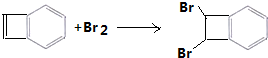
 +2CH3CH2OH$?_{��}^{Ũ����}$
+2CH3CH2OH$?_{��}^{Ũ����}$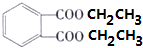 +2H2O
+2H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ��������Ӧ�����ƶ� | B�� | a+b��c+d | ||
| C�� | C������������� | D�� | B��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
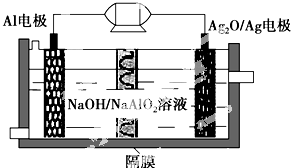 Al-Ag2O�����һ�ֿ�����ˮ�¶�����������Դ����ԭ����ͼ��ʾ���õ�ع���ʱ�ܷ�ӦʽΪ2Al+3Ag2O+2NaOH�T2NaAlO2+6Ag+H2O��������˵��������ǣ�������
Al-Ag2O�����һ�ֿ�����ˮ�¶�����������Դ����ԭ����ͼ��ʾ���õ�ع���ʱ�ܷ�ӦʽΪ2Al+3Ag2O+2NaOH�T2NaAlO2+6Ag+H2O��������˵��������ǣ�������| A�� | ����ʱ����������ԭ��Ӧ | |
| B�� | ���缫������1.08 g Agʱ����·��ת�Ƶĵ���Ϊ0.01 mol | |
| C�� | Al�缫�ķ�ӦʽΪAl-3e-+4OH-=AlO2-+2H2O | |
| D�� | ����ʱ���Һ�е�Na+����Ĥ����Al�缫�ŵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
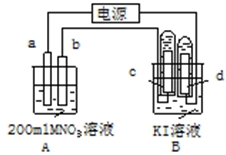 ��ͼװ���У�b�缫�ý���M�Ƴɣ�a��c��dΪʯī�缫����ͨ��Դ������M������b����ͬʱa��d�缫�ϲ������ݣ��Իش�
��ͼװ���У�b�缫�ý���M�Ƴɣ�a��c��dΪʯī�缫����ͨ��Դ������M������b����ͬʱa��d�缫�ϲ������ݣ��Իش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com