
【题目】已知在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)图示装置有两处重要组成部分未画出,它们是____________ 、_______________。
(2)烧杯间填满碎泡沫塑料的作用是 ________________。
(3)若操作时分几次注入反应液,求得的反应热数值_____(填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用__________次。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c= 4.18 J/(g℃)。请列式计算中和热:△H= ______________kJ/mol(不用化简)。
【答案】 硬纸板 环形玻璃搅拌棒 减少实验过程中热量损失 偏小 3 -0.418(t2-t1)/0.025或 -16.72(t2-t1)
【解析】(1)图示装置有两处重要组成部分未画出,它们是盖在烧杯口的硬纸板和用于搅拌的环形玻璃搅拌棒。
(2)烧杯间填满碎泡沫塑料的作用是减少实验过程中热量损失。
(3)若操作时分几次注入反应液,则每次打开硬纸板加注反应液时,都会有热量损失,所以求得的反应热数值偏小。
(4)做一次完整的中和热测定实验,温度计需使用3次,分别是测反应前酸溶液的温度、测反应前碱溶液的温度以及混合反应后测最高温度。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,则混合后溶液的质量为100g,生成水0.025mol,中和热△H=![]() -0.418(t2-t1)/0.025 kJ/mol。
-0.418(t2-t1)/0.025 kJ/mol。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________kJ·mol-1。
Ⅱ.2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________,E表示______________;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甲烷和Cl2的反应与乙烯和Br2的反应属于同一有机反应类型
B. 单质硅是将太阳能转化为电能的常用材料
C. 淀粉、纤维素和油脂都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业的基本原理就是电解饱和食盐水。下列关于实验室电解饱和食盐水的说法中正确的是( )
A. 可以选用石墨棒作为阴、阳极材料,但阳极材料也可以用铁棒
B. 用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝
C. 电解过程中,在阳极区域溶液中滴加品红,品红褪色
D. 实验结束后,将溶液搅拌,然后用pH试纸检验,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请结合下图回答问题: 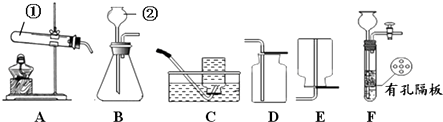
(1)写出有标号的仪器名称:① , ② .
(2)实验室用高锰酸钾制取O2的化学方程式为 , 用A、C装置制取O2时,为防止高锰酸钾进入导管,可采取的措施是 .
(3)实验室用B、D装置制取CO2的化学方程式为 , 若将发生装置由B改为F,其优点是 .
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水.SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气.用下图所示装置收集一瓶干燥的SO2 , 装置中导管按气流方向连接顺序是→⑤(填序号);图中漏斗的作用是;烧杯中NaOH溶液的作用是(用化学方程式表示). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2 (g)+O2(g)![]() 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )

A. 图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D. 图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com