
Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ���
I���Ʊ�Na2S2O35H2O ��Ӧԭ����Na2SO3��aq��+S��s�� Na2S2O3(aq)
Na2S2O3(aq)
ʵ�鲽�裺
�ٳ�ȡ15g Na2SO3����Բ����ƿ�У��ټ���80ml����ˮ����ȡ5g��ϸ����ۣ���3ml�Ҵ���ʪ������������Һ�С�
�ڰ�װʵ��װ�ã���ͼ��ʾ�����ּӳ�װ����ȥ����ˮԡ���ȣ���60���ӡ�

�۳��ȹ��ˣ�����Һˮԡ����Ũ������ȴ����Na2S2O35H2O�������ˣ�ϴ�ӣ�����õ���Ʒ��
�ش����⣺
��1������a�������� ���������� ��
��2����Ʒ�г�����δ��Ӧ��Na2SO3�⣬����ܴ��ڵ��������� �������Ƿ���ڸ����ʵķ����� ��
��3����ʵ��һ������ڼ��Ի����½��У������Ʒ���ƣ������ӷ���ʽ��ʾ��ԭ�� ��
II.�ⶨ��Ʒ����
ȷ��ȡWg��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0.1000 molL1��ı���Һ�ζ����ζ����յ�ʱ�����ı���Һ�����Ϊ18.10 mL��
��Ӧԭ��Ϊ��2S2O32+I2=S4O62-+2I
��4���ζ����յ�ʱ����Һ��ɫ�ı仯�� ��
��5����Ʒ�Ĵ���Ϊ����Na2S2O35H2O��Է�������ΪM�� ��
III.Na2S2O3��Ӧ��
��6��Na2S2O3��ԭ�Խ�ǿ������Һ���ױ�Cl2������SO42�����������������÷�Ӧ�����ӷ���ʽΪ ��
(1) ������ ��������
(2) Na2SO4 ȡ������Ʒ���ڹ������ᣬ���ˣ�����Һ�м�BaCl2��Һ�����а�ɫ���������Ʒ�к���Na2SO4
(3) S2O32-��2H��===S����SO2����H2O
(4) ����ɫ����ɫ
(5) 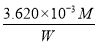 ��100%
��100%
(6) S2O32-��4Cl2��5H2O===2SO42-��8Cl����10H��
��������
���������(1)װ��������a�������ܣ����������������ķ�Ӧ������á�(2)��Ӧ��Na2SO3�ױ������е�����������Na2SO4���ʿ��ܴ��ڵ���������Na2SO4�������Ʒ���Ƿ���Na2SO4��������SO42-�Ƿ���ڣ���Ҫ��ֹSO32-�ĸ��ţ��ʲ����þ���ǿ�����Ե������ữ����Ӧ�������ữ�����˳�ȥ�����������Һ�еμ��Ȼ�����Һ�� (3)��Ʒ���ƣ�˵����Ʒ�к��������ʣ��������������Ի�����Na2S2O3���ȶ��������绯��Ӧ��2H����S2O32-===S����SO2����H2O���¡�(4)�ζ��յ�ʱ�������ĵ��ʵ�ʹ��ɫ�ĵ�����Һ��������ָʾ�ζ��յ㡣
(5)��ʼ����Ϊ0.00 mL���յ����Ϊ18.10 mL���������ĵ�ı���Һ�����Ϊ18.10 mL��0.00 mL��18.10 mL������2Na2S2O3��5H2O��2S2O32-��I2����n(Na2S2O3��5H2O) ��2n(I2)��2��0.100 0 mol��L��1��18.10��10��3 L��3.620��10��3 mol�����Ʒ�Ĵ���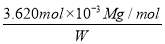 ��100%��
��100%��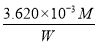 ��100%�� (6) S2O32-��Cl2������SO42-��Cl2����ԭΪCl�������ȸ��ݻ��ϼ������������д��S2O32-��4Cl2��2SO42-��8Cl����Ȼ�����ԭ���غ�͵���غ�д��S2O32-��4Cl2��5H2O===2SO42-��8Cl����10OH����
��100%�� (6) S2O32-��Cl2������SO42-��Cl2����ԭΪCl�������ȸ��ݻ��ϼ������������д��S2O32-��4Cl2��2SO42-��8Cl����Ȼ�����ԭ���غ�͵���غ�д��S2O32-��4Cl2��5H2O===2SO42-��8Cl����10OH����
���㣺 �˽⺬��������ʡ��˽�������ԭ��Ӧ�ı����ǵ��ӵ�ת�ơ��˽ⳣ����������ԭ��Ӧ�����ճ���������ԭ��Ӧ����ƽ����ؼ��㡣 ��ʶ��������������ʵ�����ʶ����͵�ʵ������װ��ͼ��


 �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ���ŵ���У�߶���ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
����װ�û�����ܴﵽĿ�ĵ���
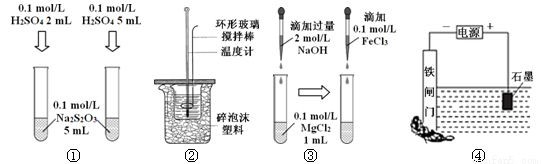
A��װ�â�̽��H2SO4Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
B��װ�âڿ����ڲⶨ�к���
C��װ�â�̽��Mg(OH)2�ܷ�ת����Fe(OH)3
D��װ�âܿɱ�����բ�Ų�����ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�һ��ѧ�����п��Ի�ѧ���������棩 ���ͣ������
��6*1�֣���������98%��ŨH2SO4����=1.84 g/cm3�����Ƴ�0.5 mol/L��ϡH2SO4 500 mL�IJ������밴Ҫ����գ�
��1��Ũ��������ʵ���Ũ��Ϊ ��
��2������ŨH2SO4�����Ϊ ��
��3������ȡ��ŨH2SO4���ձ��ڱ�����ע��ʢ��Լ100 mLˮ�� ������Ͻ��衣
��4����ȴ��������Һת�Ƶ� �У�������ˮϴ���ձ�2��3�Σ�����ϴ��Һע������ƿ�С�
��5����ˮ����̶� �������� ��ˮ��ʹ��Һ�İ�Һ�����ø��̶���ƽ��ҡ�ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�һ��ѧ�����п��Ի�ѧ���������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ȷ����
A. ����þ��ϡ���ᷴӦ ��Mg+2H++2Cl��===MgCl2+H2��
B. �Ȼ�����Һ�����ᷴӦ ��Ba2++ SO ===BaSO4��
===BaSO4��
C. ̼������Һ�����ᷴӦ ��Na2CO3+2H+===2Na++H2O+CO2��
D. ������þ��������Һ��Ӧ��OH��+H+===H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�һ��ѧ�����п��Ի�ѧ���������棩 ���ͣ�ѡ����
��������������������ȷ����
A�������в�һ��������Ԫ�� B��������һ��������Ԫ��
C���ڷ�Ӧ��ʧȥ���ӵ����� D���ڷ�Ӧ�л��ϼ����ߵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и����������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�±���������֮��ͨ��һ����Ӧ����ʵ������ʾת������

����ѡ�� | a | b | c | m |
A | N2 | NO | HNO3 | O2 |
B | Cl2 | FeCl3 | FeCl2 | Fe |
C | Na2CO3 | NaHCO3 | NaOH | CO2 |
D | CH3CH2OH | CH3CHO | CH3COOH | O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и����������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ijԭ���װ����ͼ��ʾ������ܷ�ӦΪ��2Ag��Cl2��2AgCl������˵����ȷ����

A��������ӦΪAgCl ��e����Ag ��Cl��
B���ŵ�ʱ������Ĥ�Ҳ���Һ���д�����ɫ��������
C������NaCl��Һ�������ᣬ�����ܷ�Ӧ��֮�ı�
D������·��ת��0.01 mol e��ʱ������Ĥ�����Һ��Լ����0.02 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������һ�����У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ijһ�����з������·�Ӧ��2NO(g)��O2(g)  2NO2(g)�� ��H = Q kJ��mol��1��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)�����¶ȱ仯�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����
2NO2(g)�� ��H = Q kJ��mol��1��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)�����¶ȱ仯�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����

A��p2 > p1 ��Q <0
B��p2 > p1 ��Q >0
C��p2 < p1 ��Q <0
D��p2 < p1 ��Q >0
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com