
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )。
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42- 向Cu极移动
④若有0.5 mol电子流经导线,则可产生0.25 mol气体
⑤电子的流向是:Cu―→Zn
⑥正极反应式:Cu+2e-===Cu2+,发生氧化反应
A.①②③ B.②④⑥ C.③④⑤ D.②④
科目:高中化学 来源: 题型:
在一定温度下发生可逆反应A(g)+3 B(g) 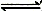 2C(g),下列叙述中不能判断该反应达到平衡状态的是( )
2C(g),下列叙述中不能判断该反应达到平衡状态的是( )
A.C的生成速率与C的分解速率相等
B.单位时间内生成amolA,同时生成3amolB
C.A、B、C的浓度不再变化
D.单位时间内消耗amolA,同时生成3amolB
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是 ( )
A.因为Fe3+具有氧化性,所以用KSCN溶液可以鉴别Fe3+ (2013·广东理综,10B)
B.工业上利用合成氨实现人工固氮不涉及氧化还原反应 (2012·广东理综,10C)
C.Na2O2用作呼吸面具的供氧剂不涉及氧化还原反应 (2012·广东理综,10A)
D.实验室用NH4Cl和Ca(OH)2制备NH3不涉及氧化还原反应 (2012·广东理综,10D)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可由软锰矿(主要成分为MnO2)制备KMn O4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
O4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(1)用软锰矿制备K2MnO4的化学方程式是___________________________________。
(2)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为__________________。生成0.1 mol还原产物时转移电子__________个。KMnO4、K2MnO4和MnO2的氧化性由强到弱的顺序是__________________________________。
(3)KMnO4能与热的Na2C2O4(aq ,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品 0.165 g,能与0.335 g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为________________________________________________。
,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品 0.165 g,能与0.335 g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若先通入另一种气体,再通入SO2,则可生成白色沉淀。另一种气体不可能是( )。
A.NO2 B.Cl2 C.HCl D.NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )。
A.X的原子半径一定大于Y的原子半径
B.X与Y的简单离子不可能具有相同的电子层结构
C.两元素形成的化合物中,原子个数比不可能为1 :1
D.X2Y可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
利用NO2平衡气体遇热颜色加深、遇冷颜色变浅来指示放热过程和吸热过程。

①按图所示将实验装置连接好。
②向甲烧杯的水中投入一定量的CaO固体,此烧杯中的NO2平衡混合气体的红棕色变深;向乙烧杯中加入NH4NO3晶体,此时烧杯中NO2平衡混合气体颜色变浅。回答下列问题:
(1)CaO与水反应的化学方程式为 _,
该反应为________ __ _ _(填“吸热反应”或“放热反应”)。
(2)NH4NO3晶体溶于水温度________(填“升高”或“降低”);NH4NO3溶于水_____ ______ (填“是”或“不是”)吸热反应。
(3)查阅资料知NO2的平衡气体中存在的可逆反应为2NO2(g) N2O4(g),已知NO2为红棕色,N2O4为无色,结合实验知,当温度升高时,平衡__ _ _____(填“未被破坏”或“发生移动”),此时反应速率________(填“增大”、“减小”或“不变化”)。混合气体的颜色不变______(填“能”或“不能”)证明反应已达平衡。
N2O4(g),已知NO2为红棕色,N2O4为无色,结合实验知,当温度升高时,平衡__ _ _____(填“未被破坏”或“发生移动”),此时反应速率________(填“增大”、“减小”或“不变化”)。混合气体的颜色不变______(填“能”或“不能”)证明反应已达平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的总反应为:
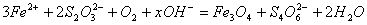 。下列说法正确的是( )。
。下列说法正确的是( )。
A.Fe2+、S2O32-都是还原剂 B.每生成1 mol Fe3O4,则转移电子数为3 mol
C.硫元素被氧化,铁元素被还原 D. x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,各容器中盛有海水,铁在其中被腐蚀时,由快到慢的顺序是( )

A.4>2>1>3 B.2>1>3>4
C.4>2>3>1 D.3>2>4>1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com