
| A. | 3:8 | B. | 32:21 | C. | 21:32 | D. | 21:8 |
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{ab}{2V}$mol.L-1 | B. | $\frac{ab}{2000V}$mol.L-1 | C. | $\frac{250ab}{V}$mol.L-1 | D. | $\frac{ab}{80V}$mol.L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L氦气中原子数为NA | |
| B. | 常温常压下,1.06gNa2CO3中阴离子电荷数为0.02NA | |
| C. | 标准状况下,22.4LCCl4中的分子个数为NA | |
| D. | 0.5mol/L的MgCl2溶液中的氯离子个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 剩余固体一定有铜 | B. | 反应后的溶液呈蓝色 | ||
| C. | 剩余固体中一定有银 | D. | 反应后的溶液为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,固体的量减少 | |
| B. | 加入少量Na2CO3粉末能增大钙离子的浓度 | |
| C. | 恒温下加入少量CaO,溶液的pH增大 | |
| D. | 降低温度,溶液中c(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
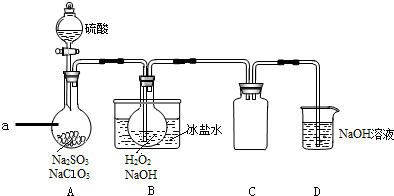
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0mol | B. | 1mol | C. | 2mol | D. | 3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HNO3具有氧化性 | B. | NH3既具有氧化性又具有还原性 | ||
| C. | N2只具有还原性 | D. | NO2既具有氧化性又具有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com