
�±���3�����ʵ��ܽ�ȣ�20�棩������˵������ȷ���ǣ� ��
���� | MgCl2 | Mg��OH��2 | MgCO3 |
�ܽ�ȣ�g/100g�� | 74 | 0.000 84 | 0.01 |
A����֪MgCO3��Ksp=6.82��10��6 mol2��L��2�������к��й���MgCO3����Һ�У�����c��Mg2+��=c��CO32��������c��Mg2+����c��CO32����=6.82��10��6 mol2��L��2
B����ȥ�����к��е�MgCl2���ʣ���ѳ����Լ�ΪNa2CO3��Һ
C������������������ˮ��ϣ����ȡ����գ����յĹ��������ͬ
D����ʯ��ˮ��������Mg2+��HCO3����Ӳˮ�����������ӷ�Ӧ����ʽΪMg2++2HCO3��+Ca2++2OH���TCaCO3��+MgCO3��+2H2O
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017������ʡ������ģ��һ��ѧ�Ծ��������棩 ���ͣ������
��ҵ�Ͽ������÷����е�CO2Ϊԭ����ȡ�״�����ش��������⣺
(1) ��֪���³�ѹ�£������������淴Ӧ�������仯����ͼ��ʾ��
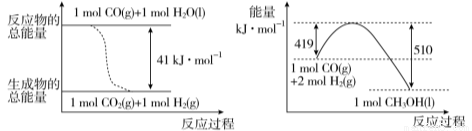
��д����ͼ��Ӧ��ƽ�ⳣ������ʽK= ��
��д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ ��
(2) ���ֻ�ı�һ������ʹ������Ӧ����ʽ��ƽ�ⳣ��Kֵ�����÷�Ӧ________(ѡ����)��
A��һ��������Ӧ�����ƶ� B����ƽ���ƶ�ʱ������Ӧ������������С
C��һ�����淴Ӧ�����ƶ� D����ƽ���ƶ�ʱ���淴Ӧ�����ȼ�С������
(3) �������������������£����������ѹ����ԭ����1/2����ԭƽ����ȣ������й�˵����ȷ����________(����ĸ)��
A��H2��Ũ�ȼ�С B������Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
C���״������ʵ������� D������ƽ��ʱ��n(H2)/n(CH3OH)����
(4) �����¶Ⱥ�������䣬ͨ��1molCO2��3molH2 ��������˵���÷�Ӧ�Ѵ�ƽ��״̬����________(����ĸ)��
��������˵���÷�Ӧ�Ѵ�ƽ��״̬����________(����ĸ)��
A��n(CO2)��n(H2)��n(CH3OH)��n(H2O)��1��3��1��1
B��������ѹǿ���ֲ���
C��H2������������CO2����������֮��Ϊ3��1
D�������������ƽ����Է����������ֲ���
(5) ����Ӧ�������ݻ�Ϊ2.0 L����Ӧʱ��4.0 min������ ��������ܶȼ�����2.0 g��L-1�������ʱ����CO2��ƽ����Ӧ����Ϊ_______________
��������ܶȼ�����2.0 g��L-1�������ʱ����CO2��ƽ����Ӧ����Ϊ_______________
(6) ������Ƽ״�-����ȼ�ϵ�ص�Դ�� ��ʯī���缫���200 mL�����������ӵ���Һ��
��ʯī���缫���200 mL�����������ӵ���Һ��
���� | Cu2+ | H+ | Cl- | SO |
c/(mol��L-1) | 0.5 | 2 | 2 | 0.5 |
���һ��ʱ�����µ������ռ�����ͬ���������ʱ���������ռ�������������Ϊ____________(������Һ����ı仯���缫������ܴ��ڵ��ܽ�����)��Ҳ�����ô˵�Դ���õ�ⷨ�Ʊ�Na2FeO4����������Ϊ������������Һ��NaOH��Һ��������ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʦ���и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������͢����ȷ���������ϵ����( )
ѡ�� | ������ | ������ |
A | 1?�����ķе�ȼ���ķе�� | 1?�����ͼ����ͨ������������� |
B | ԭ��ؿɽ���ѧ��ת��Ϊ���� | ԭ�������ӵ�Դ���ܹ��� |
C | �Ҷ������KMnO4��Һ������Ӧ | �Ҷ���������� |
D | Na��Cl2��ȼ�յ������ﺬ���Ӽ� | NaCl����ɵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ�����л�ѧ���������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������������ȷ����( )
A��1 mol CH3����������Ϊ10NA
B��1 mol Na2O��Na2O2�����������������������3NA
C����״���£�22.4 Lˮ�к���ԭ������Ϊ3NA
D��1molCl2��ȫ����ˮ��ת�Ƶĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ¦���е���У�߶������л�ѧ���������棩 ���ͣ�ʵ����
��1����һѧ����ʵ���Ҳ�ij��ҺpH��ʵ��ʱ������������ˮ��ʪpH��ֽ��Ȼ���ýྻ����IJ�����պȡ�������м�⡣
�����ִ������ ���һ����/��һ������/����һ�������ᵼ��ʵ��������
�������˷��ֱ�ⶨc(H+)��ȵ�����ʹ�����Һ��pH�����ϴ���� ��
��2��������֪Ũ�ȵ� NaOH ��Һ�ⶨij HCl��Һ��Ũ�ȣ��ο���ͼ���ӱ���ѡ����ȷ���
��� | ��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� |
|
A | �� | �� | ʯ | ���ң� |
B | �� | �� | ��̪ | ���ף� |
C | �� | �� | ���� | ���ף� |
D | �� | �� | ��̪ | ���ң� |
(3)���ñ���NaOH�ζ�δ֪Ũ�ȵ����ᣬѡ�÷�̪Ϊָʾ������ɲⶨ���ƫ�ߵ�ԭ������� ��
A�����Ʊ���Һ�����������л���Na2CO3����
B���ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�������������ȷ
C��ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
D���ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
E��δ�ñ�Һ��ϴ��ʽ�ζ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ¦���е���У�߶������л�ѧ���������棩 ���ͣ�ѡ����
���жԡ��ı䷴Ӧ����,���»�ѧ��Ӧ���ʸı䡱��ԭ����������ȷ����
A������Ӧ���Ũ�ȣ�����Ӱٷ������ӣ���Ӧ���ʼӿ�
B���������巴Ӧ��ϵ��ѹǿ����λ����л���������࣬���巴Ӧ���ʼӿ�
C�����߷�Ӧ���¶ȣ�����Ӱٷ������ӣ���Ч��ײ�ļ�����ߣ���Ӧ��������
D������ͨ���ı䷴Ӧ·����ʹ��Ӧ����Ļ�ܽ��ͣ���Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ¦���е���У�߶������л�ѧ���������棩 ���ͣ�ѡ����
��ӦA(g)+B(g) C(g)+D(g)���������е������仯��ͼ����H��ʾ��Ӧ���ʱ䡣����˵����ȷ����
C(g)+D(g)���������е������仯��ͼ����H��ʾ��Ӧ���ʱ䡣����˵����ȷ����
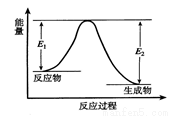
A����Ӧ��ϵ�м����������Ӧ ��������E1��С��E2����
��������E1����E2����
B����Ӧ��ϵ�м����������Ӧ��������H����
C����H < 0����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת��������
D����H > 0����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ����������У��һ����������ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ�У����ܴ���������������ǣ� ��AC
A��Cu2+��Na+��SO42-��Cl- B��K+��Na+��HCO3-��NO3-
C��OH-��HCO3-��Ca2+��Na+ D��Ba2+��Na+��OH-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������������ʱ���ı�ijһ�����Է�ӦA2(g)+3B2(g) 2AB3(g)�Ļ�ѧƽ��״̬��Ӱ��������ͼ��ʾ��T��ʾ�¶ȣ�n��ʾ���ʵ������������ж���ȷ���ǣ� ��
2AB3(g)�Ļ�ѧƽ��״̬��Ӱ��������ͼ��ʾ��T��ʾ�¶ȣ�n��ʾ���ʵ������������ж���ȷ���ǣ� ��

A����Ӧ���ʣ�a>b>c
B���ﵽƽ��ʱA��ת���ʴ�С��b>a>c
C����T2>T1��������Ӧһ�������ȷ�Ӧ
D���ﵽƽ��ʱ��n( AB3)�Ĵ�С��b>a>c
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com