
| A. | 向装有Fe(NO3)2溶液的试符中加入稀H2SO4,在管口观察到红棕色气体,结论:HNO3分解成了NO2 | |
| B. | 高温下用焦炭还原SiO2制取粗硅 | |
| C. | Na2O2用作呼吸面具的供氧裒剂涉及氧化还原反应 | |
| D. | 浓硝酸有强氧化性,常温下能与Fe发生剧烈反应 |
分析 A.NO3-在酸性条件下具有氧化性,被还原生成NO,NO被O2氧化为红棕色的NO2;
B、高温下炭与二氧化硅反应生成一氧化碳和粗硅;
C、过氧化钠与二氧化碳反应生成碳酸钠和氧气,过氧化钠中O元素的化合价变化;
D、铁与浓硝酸发生钝化现象.
解答 解:A.向Fe(NO3)2溶液中加入H2SO4,则会发生离子反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,产生的NO在管口生成NO2呈现红色,而不是HNO3分解产生NO2,故A错误;
B、高温下炭与二氧化硅反应生成一氧化碳和粗硅,故B正确;
C、过氧化钠与二氧化碳反应生成碳酸钠和氧气,过氧化钠中O元素的化合价变化,所以涉及氧化还原反应,故C正确;
D、铁与浓硝酸发生钝化现象,而不是剧烈反应,故D错误;
故选BC.
点评 本题考查元素化合物知识,为高频考点,把握发生的反应、反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | pH=2的硫酸溶液含有H+数目为0.0lNA | |
| B. | 该反应释放SO2分子数目为$\frac{V}{22.4}$NA | |
| C. | 反应中每摩尔Na2S2O3转移的电子数目为4NA | |
| D. | 若98gH2SO4溶于水完全电离,其断裂的共价键数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
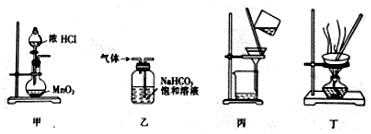
| A. | 用装置甲完成实验室制取氯气 | |
| B. | 用装置乙除去二氧化碳中的少量氯化氢 | |
| C. | 用装置丙分离二氧化锰和氯化锰溶液 | |
| D. | 用装置丁蒸干碳酸氢钠溶液制NaHCO3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 物品标签 |  |  |  |  |
| 分析 | 该试剂应装在橡 胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 受热易分解 | 该药品标签上还标有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu 溶于稀 HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用CH3COOH溶解 CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | FeCl3溶液与Cu反应:2Fe3++Cu═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3易溶于水,可用作净水剂 | |
| B. | 硅是半导体材料,纯净的硅是光纤制品的基本原料 | |
| C. | 浓硫酸能干燥氯气,说明浓硫酸具有吸水性 | |
| D. | 氨易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
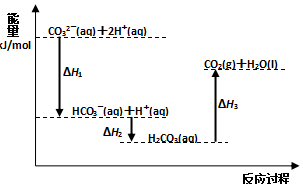
| A. | 反应HCO3-(aq)+H+(aq)=CO2(g)+H2O(l) 为放热反应 | |
| B. | CO32-(aq)+2H+(aq)=CO2(g)+H2O(l)△H=(△H1+△H2+△H3) | |
| C. | △H1>△H2△H2<△H3 | |
| D. | H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则△H3变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuFeS2中硫的化合价为-1价 | |
| B. | Fe2O3为氧化产物,SO2是还原产物 | |
| C. | lmolCuFeS2反应转移电子为13mol | |
| D. | 该反应的所有产物均既是氧化产物,又是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化合物CaCl2中,除了有Ca2+与Cl-之间的离子键外,还有两个Cl-之间的共价键 | |
| B. | 碘受热升华时共价键被破坏 | |
| C. | 熔化状态下能导电的化合物中一定存在离子键 | |
| D. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com