
【题目】A、B、C、X、Y、Z、E为前四周期元素,且原子序数依次增大。A原子核外有三个能级,且每个能级上的电子数相等,C原子成对电子数是未成对电子数的3倍,X、Y、Z、E是位于同一周期的金属元素,X、E原子的最外层电子数均为1,Y有“生物金属”之称,Y4+和氩原子的核外电子排布相同,Z原子核外电子的运动状态数目是最外层电子数的14倍。用元素符号回答下列问题:
(1)B的电子排布式:_____________,Y的价电子排布图____________,Z2+的价电子排布式____________。
(2)E元素位于周期表第________周期__________族_________区。
(3)①A、B、C三种元素的第一电离能由小到大的顺序为_____________。
②A、C元素气态氢化物的稳定性的大小_________>________(分子式表示)原因_____________。
③与AC32-互为等电子体的离子_______(写一种),写出与ABC-离子互为等电子体的分子的化学式:______(写一种)。
④AC2的电子式___________。
【答案】1s22s22p3 ![]() 3d8 四 IB ds C<O<N H2O CH4 氧元素的非金属性强于碳或氧的原子半径比碳原子半径小,键长越小键能越大越稳定 NO3- N2O或CO2
3d8 四 IB ds C<O<N H2O CH4 氧元素的非金属性强于碳或氧的原子半径比碳原子半径小,键长越小键能越大越稳定 NO3- N2O或CO2 ![]()
【解析】
A、B、C、X、Y、Z、E为前四周期元素,且原子序数依次增大。A原子核外有三个能级,且每个能级上的电子数相等,A原子核外电子排布为1s22s22p2,则A为碳元素。X、Y、Z、E是位于同一周期的金属元素,元素只能处于第四周期,Y有“生物金属”之称,Y4+和氩原子的核外电子排布相同,Y元素原子核外电子数=18+4=22,故Y为Ti元素;X原子的最外层电子数为1,且X的原子序数小于Ti,故X为K元素;Z原子核外电子的运动状态数目是最外层电子数的14倍,最外层电子数只能为2,故Z原子核外电子数为28,则Z为Ni元素;E原子的最外层电子数为1,原子序数又大于Ni,则E原子的价电子排布式为3d104s1,则E为Cu元素;C原子成对电子数是未成对电子数的3倍,原子序数又小于X(钾),未成对电子数最大为3,故C原子核外电子排布式为1s22s22p4,则C为O元素;而B的原子序数介于碳、氧之间,所以B为N元素,据此分析解答。
根据上述分析可知A是C,B是N,C是O,X是K,Y是Ti,Z是Ni,E是Cu元素。
(1)B是N元素,原子序数是7,根据构造原理可知N原子的核外电子排布式为:1s22s22p3;Y是22号Ti元素,价电子排布式是3d24s2,价电子排布图为:![]() ;Z是Ni,Ni原子失去最外层的2个电子变为Ni2+,Ni2+的价电子排布式3d8;
;Z是Ni,Ni原子失去最外层的2个电子变为Ni2+,Ni2+的价电子排布式3d8;
(2)E是Cu,原子核外电子排布式是1s22s22p63s23p63d104s1,在元素周期表中位于第四周期第IB族,属于ds区;
(3)①A是C,B是N,C是O,一般情况下,同一周期的元素,随原子序数的增大,元素的第一电离能呈增大趋势,但由于N原子的2p电子处于半充满的稳定状态,所以其第一电离能比O大,则三种元素的第一电离能由小到大的顺序为C<O<N;
②元素的非金属性越强,其相应的简单氢化物的稳定性就越强,由于元素的非金属性C<O,原子半径r(C)>r(O),所以这两种元素的相应氢化物的稳定性:H2O>CH4;
③AC32-离子为CO32-,与其互为等电子体的离子为NO3-;ABC-离子为CNO-,与其互为等电子体的分子的化学式为N2O或CO2。
④AC2是CO2,在该物质分子中,C原子与2个O原子形成四对共用电子对,使分子中每个原子都达到最外层8个电子的稳定结构,所以CO2的电子式为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是
A.在纯水中加入少量硫酸铵,可抑制水的电离.
B.升高温度,活化分子百分数一定增大,化学反应速率一定增大
C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大
D.虽然固体氯化钠不能导电,但氯化钠是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
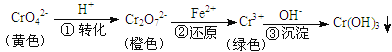
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)![]() Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
下列有关说法不正确的是
A.步骤①中当v正(CrO42—)=2v逆(Cr2O72—)时,说明反应:2CrO42—+2H+![]() Cr2O72—+H2O达到平衡状态
Cr2O72—+H2O达到平衡状态
B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原1 mol Cr2O72—离子,需要12 mol (NH4)2Fe(SO4)2
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+)≤10-5mol/L时,可视作该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________(填字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定过程中,眼睛应注视________________。滴定时,用0.2000molL-的盐酸来滴定待测液,不可选用______(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定时,用0.200 0 mol·L-1的盐酸来滴定待测溶液,根据下表数据,计算被测烧碱溶液的物质的量浓度是________ mol·L-1,烧碱样品的纯度是________。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果______
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15g/100 mL。莫尔法是较简单的一种测量Cl-含量的方法。现采用该法测量某市售酱油是否符合NaCl含量标准要求。实验原理如下(25℃):
Ag++Cl-=AgCl↓(白色) Ksp(AgCl)=1.8×10-23
2Ag++CrO42-=Ag2CrO4↓(砖红) Ksp(Ag2CrO4)=1.2×10-22
准确移取酱油样品5.00 mL稀释至100 mL。从其中取出10.00 mL 置于锥形瓶中,再向其中加入适量的K2CrO4溶液,以0.100 0 mol/L的硝酸银标准溶液滴定,重复实验三次。
(1)样品稀释过程中,用_____移取酱油样品,应在______中定容,还需用到玻璃仪器_______________。
(2)滴定中眼睛应注视____________,出现_____________即达到滴定终点。
(3)滴定结束时,滴定管中液面如右图所示,则读数为________。
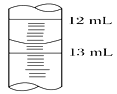
(4)若三次消耗硝酸银标准溶液的平均体积为12.50 mL,则稀释后的酱油中NaCl的浓度为________mol/L,该市售酱油是否符合NaCl含量标准 ________(填“符合”或“不符合”)。
(5)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),此离子沉淀完全(离子浓度≤10-5)时溶液的pH为________________已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=1.0×10-21。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国著名有机化学家张绪穆于2000年在JACS杂志上公布了著名的“张烯炔异构化反应”及其机理。该反应丰富了人类进行天然有机分子全合成的手段,该反应原理如下: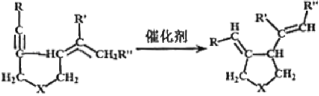
其中:—R、—R’、—R’’可以为—H、—CH3、—CH2CH3或![]() ,—X—可以为—O—、—NH—或CH2—
,—X—可以为—O—、—NH—或CH2—
现拟合成![]() 应选取的反应物是( )
应选取的反应物是( )
A.CH3—C![]() C—CH2—O—CH2—CH=CH—CH3
C—CH2—O—CH2—CH=CH—CH3
B.CH3—C![]() C—CH2—O—CH2—CH2—CH=CH2
C—CH2—O—CH2—CH2—CH=CH2
C.CH3—C![]() C—CH2—O—CH2—CH=CH—CH2—CH3
C—CH2—O—CH2—CH=CH—CH2—CH3
D.CH3—C![]() C—CH2—O—CH2—CH2—CH=CH—CH3
C—CH2—O—CH2—CH2—CH=CH—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
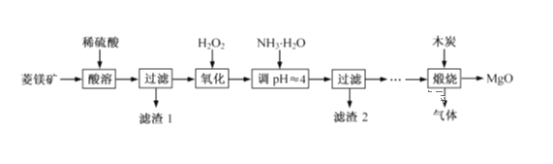
(1)MgCO3与稀硫酸反应的离子方程式为__________________________。
(2)加入H2O2氧化时,发生反应的离子方程式为__________________________。
(3)滤渣2 的成分是____________(填化学式),过滤分离需要的玻璃仪器有 __________________。
(4)煅烧过程存在以下反应:
2MgSO4+C=2MgO+2SO2↑+CO2↑
MgSO4+C=MgO+SO2↑+CO↑
MgSO4+3C=MgO+S↑+3CO↑
利用图装置对煅烧产生的气体进行分步吸收或收集。
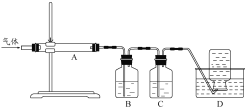
D中通过排水法收集的气体可以是___________(填化学式)。C中溶液用于吸收CO2,B中盛放的溶液可以是___________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)钢铁容易生锈的主要原因是钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。在酸性环境下,其正极反应式为_____________;在酸性很弱或中性条件下,其发生___________________ (填“析氢腐蚀”或“吸氧腐蚀”)。
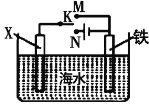
(2)利用如图装置,可以模拟铁的电化学防护。若X为碳棒,开关K置于N处,该电化学防护法称为____________________;若X为锌棒,开关K置于M处,________(填“能”或“不能”)达到防止铁腐蚀![]() 目的。
目的。
II.如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:

(1)甲池燃料电池的负极反应为___________________。
(2)乙池中石墨电极为___________极,发生_____________反应(填“氧化”或“还原”)写出乙池中电解总反应的化学方程式: ___________________。
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生________g沉淀,此时乙池中溶液的体积为400mL,该溶液的pH=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁和高铁酸钾都是常见的水处理剂。某兴趣小组以铁屑为原料模拟工业上制备氯化铁及进一步氧化制备高铁酸钾的流程如下:

请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是____________。
(2)“合成”阶段生成Na2FeO4的离子方程式为___________________________。
(3)为了检验“氧化”过程中所得FeCl3溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是_______(填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性KMnO4溶液进行检验,请分析方案是否合理,并说明理由:____________。
(4)常温下,若使6.4mol/LFeCl3饱和溶液不析出Fe(OH)3,需控制溶液的pH小于____。{已知该实验条件下,Ksp[(Fe(OH)3]=6.4×10-36}
(5)在不同温度和不同pH下,FeO42-的稳定性如图所示:

从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com