
用如图所示装置进行实验,下列叙述不正确的是
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应:4OH——4e—==2H2O+O2↑ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是( )
| A.甲装置中锌为负极,发生还原反应 |
| B.甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C.乙装置中铁极为阳极,电极反应式为: 2Na++2e-=2Na |
| D.乙装置中B是氯气出口,A是钠出口 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中因电化学腐蚀渐渐变暗 |
| B.当镀锡铁制品的镀层破损时,镶层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用如图所示装置进行实验,下列叙述不正确的是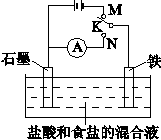
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应:4OH- - 4e- = 2H2O + O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
按下左图装置实验,若右图中x轴表示流入阴极的电子的物质的量,则y轴可表示的物理量为
①c(Ag+)②c(NO—3)③a棒的质量④b棒的质量⑤溶液的pH
| A.①③ | B.③④ | C.①②④ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电浮选凝聚法处理酸性污水的工作原理如图。下列说法不正确的是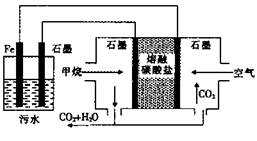
| A.铁电极的电极反应式为:Fe—2e—=Fe2+ |
| B.通人甲烷的石墨电极的电极反应式为:CH4+4CO32——8e—=5CO2+2H2O |
| C.为增强污水的导电能力,可向污水中加人适量工业用食盐 |
| D.若左池石墨电极产生44.8L气体,则消耗0. 5 mol甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢镍电池是可充电电池,总反应式是H2+2NiO(OH) 2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
A.该电池所用的电解质溶液为酸性溶液
B电池充电时,氢元素被还原
C.电池放电时,镍元素被氧化
D.该电池的负极反应为H2-2e-=2H+
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
海水淡化的方法有多种,如蒸馏法、电渗析法等。电渗析法是一种利用离子交换膜进行离子交换的方法,其原理如图所示。己知海水中含Na+、Cl—、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。下列叙述中正确的是
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子往a电极处运动 |
| C.通电后,a电极的电极反应式为:4OH--4e-=O2↑+2H2O |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图装置中,在U形管底部盛有CCl4,分别在U形管两端小心倒入饱和食盐水和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述中错误的是( )
| A.铁丝在两处的腐蚀速率:a < b |
| B.a、b两处相同的电极反应式为Fe - 2e- = Fe2+ |
| C.一段时间后,a处液面高于b处液面 |
| D.生铁丝中的碳在a、b两处分别作原电池的负极和正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com