
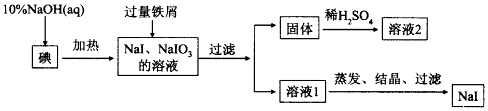
·ÖĪö ÓÉÖʱøĮ÷³ĢæÉÖŖ£¬µāÓėNaOHČÜŅŗ·“Ӧɜ³ÉNaI”¢NaIO3£¬¼ÓČėFeÓėNaIO3·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉNaI”¢ĒāŃõ»ÆĢś£¬¾¹żĀĖŗóµĆµ½ŗģŗÖÉ«¹ĢĢåĒāŃõ»ÆĢś£¬¹żĀĖŗóČÜŅŗÖŠÖ÷ŅŖŗ¬NaI£¬·ÖĄė”¢Ģį“æµĆµ½NaI£¬
£Ø1£©µāÓėĀČĪ»ÓŚĶ¬Ņ»Ö÷×壬ŗĖĶāÓŠ5øöµē×Ó²ć£»
£Ø2£©Éś³ÉIO3-ÓėIO-£¬IŌŖĖŲµÄ»ÆŗĻ¼Ū¾łÉżøߣ¬Ōņ»¹Éś³ÉNaI£¬½įŗĻµē×Ó”¢µēŗÉŹŲŗć·ÖĪö£»
£Ø3£©FeÓėNaIO3·¢ÉśŃõ»Æ»¹Ō·“Ó¦£»
£Ø4£©ÓÉČÜŅŗŗ¬H+£¬¹ĢĢåĶźČ«Čܽā£¬FeÓėĮņĖįĢś·“Ӧɜ³ÉĮņĖįŃĒĢś£»
£Ø5£©æÉÓĆÕō·¢µÄ·½·ØµĆµ½¾§Ģ壮
½ā“š ½ā£ŗ£Ø l £©µāŗĖĶāÓŠ×īĶā²ćµē×ÓŹżĪŖ7£¬5øöµē×Ó²ć£¬ŌņĪ»ÓŚÖÜĘŚ±ķµŚĪåÖÜĘŚ”¢µŚ¢÷A×壬¹Ź“š°øĪŖ£ŗµŚĪåÖÜĘŚ”¢µŚ¢÷A×壻
£Ø2£©NaOHČÜŅŗŗĶµā·“Ó¦Ź±ĖłµĆČÜŅŗÖŠIO3-ÓėIO-µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£¬Čō¾łĪŖ1mol£¬Óɵē×ÓŹŲŗćæÉÖŖ£¬Éś³ÉI-ĪŖ$\frac{1”Į5+1”Į1}{£Ø1-0£©}$=6mol£¬½įŗĻµēŗÉŹŲŗć¼°Ō×ÓŹŲŗćæÉÖŖĄė×Ó·“Ó¦ĪŖ4I2+8OH-=IO3-+IO-+6I-+4H2O£¬
¹Ź“š°øĪŖ£ŗ4”¢8”¢l”¢l”¢6”¢4£»
£Ø3£©¼ÓČė¹żĮæĢśŠ¼µÄÄæµÄŹĒ½«NaIO3ĶźČ«×Ŗ»ÆĪŖNaI£¬¼ÓČėĢśŠ¼Ź±·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3H2O+2Fe+NaIO3=NaI+2Fe£ØOH£©3”ż£¬
¹Ź“š°øĪŖ£ŗ½«NaIO3ĶźČ«×Ŗ»ÆĪŖNaI£»3H2O+2Fe+NaIO3=NaI+2Fe£ØOH£©3”ż£»
£Ø4£©¹ĢĢåÖŠ³żŹ£ÓąĢśŠ¼Ķā£¬»¹ÓŠŗģŗÖÉ«¹ĢĢ壬¼ÓĮņĖįµĆµ½ČÜŅŗ2³żŗ¬ÓŠH+Ķā£¬¹ĢĢåĶźČ«Čܽā£¬Ņ»¶Øŗ¬ÓŠµÄŃōĄė×ÓŹĒFe2+£¬
¹Ź“š°øĪŖ£ŗFe2+£»
£Ø5£©“ÓČÜŅŗÖŠ»ńµĆ¾§Ģ壬æɽ«ČÜŅŗ½ųŠŠÕō·¢ÅØĖõ£¬Č»ŗóĄäČ“½į¾§£¬¹żĀĖµĆµ½¾§Ģ壬¹Ź“š°øĪŖ£ŗÕō·¢ÅØĖõ”¢ĄäČ“½į¾§£®
µćĘĄ ±¾Ģāæ¼²éÖʱøŹµŃé·½°øµÄÉč¼Ę£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕÖʱøĮ÷³ĢÖŠµÄ·“Ó¦¼°Ńõ»Æ»¹Ō·“Ó¦µÄ·ÖĪö”¢ÖŹĮæŹŲŗćµÄ¼ĘĖćµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬×ŪŗĻŠŌ½ĻĒ棬ĢāÄæÄѶČÖŠµČ£®


 ÓäæģµÄŗ®¼ŁÄĻ¾©³ö°ęÉēĻµĮŠ“š°ø
ÓäæģµÄŗ®¼ŁÄĻ¾©³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | 0.01mol•L-1ĖįŠŌKMnO4ČÜŅŗ | 0.1mol•L-1H2C2O4ČÜŅŗ | Ė® | 1mol•L-1MnSO4ČÜŅŗ | ·“Ó¦ĪĀ¶Č/”ę | ·“Ó¦Ź±¼ä |
| ¢ń | 2mL | 2mL | 0 | 0 | 20 | 125 |
| ¢ņ | V1 mL | V2 mL | 1mL | 0 | 20 | 320 |
| ¢ó | V3 mL | V4 mL | V5mL | 0 | 50 | 30 |
| ¢ō | 2mL | 2mL | 0 | 2µĪ | 20 | 10 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 ¢ŚŹµ¼ŹÉś²ś¹ż³ĢÖŠ¶ŌĖł¼ÓĻ”ĻõĖįµÄÅضČæŲÖĘŅŖĒó±Č½Ļøߣ¬Ķس£ÓƱź×¼ĒāŃõ»ÆÄĘČÜŅŗĄ“µĪ¶Ø£®µĪ¶Ø¹ż³ĢÖŠČōÓĆ·ÓĢŖ×÷ÖøŹ¾¼Į£¬ÖÕµćĻÖĻóŹĒČÜŅŗÓÉĪŽÉ«±ä³ÉŗģÉ«£Ø»ņĒ³ŗģÉ«£©£¬ĒŅ°ė·ÖÖÓÄŚ²»ĶŹÉ«£®ĒėŌŚĶ¼ÖŠ»³öµĪ¶Ø¹ż³ĢÖŠČÜŅŗµÄpHĖęĖłµĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗĢå»żµÄ±ä»ÆµÄĒśĻßĶ¼£ØŅŖĒó¹żAµć£©£®
¢ŚŹµ¼ŹÉś²ś¹ż³ĢÖŠ¶ŌĖł¼ÓĻ”ĻõĖįµÄÅضČæŲÖĘŅŖĒó±Č½Ļøߣ¬Ķس£ÓƱź×¼ĒāŃõ»ÆÄĘČÜŅŗĄ“µĪ¶Ø£®µĪ¶Ø¹ż³ĢÖŠČōÓĆ·ÓĢŖ×÷ÖøŹ¾¼Į£¬ÖÕµćĻÖĻóŹĒČÜŅŗÓÉĪŽÉ«±ä³ÉŗģÉ«£Ø»ņĒ³ŗģÉ«£©£¬ĒŅ°ė·ÖÖÓÄŚ²»ĶŹÉ«£®ĒėŌŚĶ¼ÖŠ»³öµĪ¶Ø¹ż³ĢÖŠČÜŅŗµÄpHĖęĖłµĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗĢå»żµÄ±ä»ÆµÄĒśĻßĶ¼£ØŅŖĒó¹żAµć£©£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ŃõĘų | B£® | µŖĘų | C£® | ¶žŃõ»ÆĢ¼ | D£® | Ļ”ÓŠĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ŹµŃéŠņŗÅ | ¢ń | ¢ņ | ¢ó | ¢ō |
| ŃĪĖįĢå»ż£ØmL£© | 30.0 | 30.0 | 30.0 | 30.0 |
| ѳʷ֏Įæ£Øg£© | 2.96 | 3.70 | 5.18 | 6.66 |
| CO2µÄĢå»ż£ØmL£© | 672 | 840 | 896 | 672 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØH+£© | B£® | Ka£ØHF£© | C£® | $\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$ | D£® | $\frac{c£Ø{H}^{+}£©}{c£ØHF£©}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü¢Ż | B£® | Ö»ÓŠ¢Ł¢Ü¢Ż | C£® | Ö»ÓŠ¢Ś¢Ū | D£® | Ö»ÓŠ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆA±ķŹ¾µÄ·“Ó¦ĖŁĀŹŹĒ0.8mol/£ØL•min£© | |
| B£® | 2minÄ©Ź±µÄ·“Ó¦ĖŁĀŹ£¬ÓĆB±ķŹ¾ĪŖ0.6mol/£ØL•min£© | |
| C£® | ÓĆC±ķŹ¾µÄ·“Ó¦ĖŁĀŹŹĒ0.4mol/£ØL•min£© | |
| D£® | ČōÓĆD±ķŹ¾·“Ó¦ĖŁĀŹŹĒ0.8mol/£ØL•min£©£¬Ōņx=2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com