
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④ C.②④ D.②③
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
实验室制取乙烯的装置如图所示,试回答:
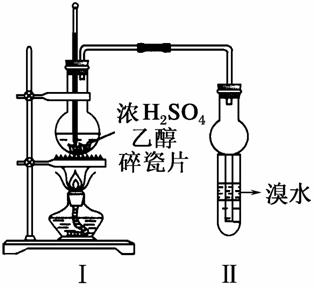
(1)烧瓶中发生反应的化学方程式为_________________________
______________________________________________________________________________________________________________。
(2)实验中发现试管Ⅱ中溴水褪色,此现象能否说明一定有乙烯生成________(填“能”或“不能”)。
试管中另一现象可证明确实有乙烯生成,该现象是__________;试管Ⅱ中溴水褪色能否说明是由于乙烯与溴水发生了加成反应________(填“能”或“不能”)。通过测定反应后溶液的pH可进一步证明是发生了取代反应还是加成反应,原因是__________________
______________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某电镀铜厂有两种废水需要处理,一种废水中含有CN-,另一种废水中含有Cr2O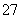 。该厂拟定如图所示的废水处理流程。
。该厂拟定如图所示的废水处理流程。

回答以下问题:
(1)上述处理废水的流程中主要使用的方法是___ _____________________________________________________________________。
_____________________________________________________________________。
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因________________________________________________________________________。
(3)②中反应后无气体放出,该反应的离子方程式为
________________________________________________________________________。
(4)③中反应时,每0.4 mol Cr2O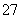 转移2.4 mol e-,该反应的离子方程式为________________________________________________________________________。
转移2.4 mol e-,该反应的离子方程式为________________________________________________________________________。
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少。请你使用化学用语,结合必要的文字解释其原因________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯与综合利用工艺如下:

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是____________________。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为________。由气体Ⅱ中某物得到水玻璃的化学反应方程式为____________________________________________。
(3)步骤①为:搅拌、________。所得溶液Ⅳ中的阴离子有________。
(4)由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为______________________________________________,100 kg初级石墨最多可能获得Ⅴ的质量为______kg。
(5)石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末
B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应
D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中的固体剩余物是( )
A.Na2CO3和Na2O2
B.Na2CO3和NaOH
C.NaOH和Na2O2
D.NaOH、Na2O2和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知丙二醇的结构简式为 ,下列关于丙二醇的说法正确的是( )
,下列关于丙二醇的说法正确的是( )
A.丙二醇可发生消去反应生成丙炔
B.丙二醇可由丙烯在一定条件下与水加成制得
C.丙烯与溴水加成后,再与NaOH醇溶液共热水解可得丙二醇
D.丙二醇在铜存在下催化氧化可得到丙二醛
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选 项 | ① | ② | ③ | 实验结论 |
|
| A. | 稀 硫 酸 | Na2S | AgNO3与 AgCl的 浊液 | Ksp(AgCl)> Ksp(Ag2S) | |
| B. | 浓 硫 酸 | 蔗糖 | 溴水 | 浓硫酸具有脱 水性、氧化性 | |
| C. | 稀 盐 酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性 钡盐均可生成 白色沉淀 | |
| D. | 浓 硝 酸 | Na2CO3 | Na2SiO3 溶液 | 酸性:硝酸> 碳酸>硅酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com