
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( ) 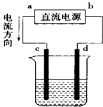
A.a为负极,b为正极
B.d为阳极,c为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:
【题目】胶体区别于其他分散系的本质特征是
A. 胶体粒子做布朗运动 B. 分散质粒子直径在10-9~10-7m之间
C. 胶体能产生丁达尔现象 D. 胶体是纯净物,气体分散系是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不符合生产实际的是( )
A.电解熔融的氧化铝制取金属铝,用铁做阳极
B.电解法精炼粗铜,用纯铜做阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网做阴极
D.在镀件上电镀锌,用锌做阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系:a A(g)+b B(g)![]() c C(g)+d D(s) △H<0,下列判断中正确的是
c C(g)+d D(s) △H<0,下列判断中正确的是
A. 若(a+b) < (c+d),则反应一定能自发向右进行
B. 若起始时只充入A、B,且物质的量之比为a:b,则平衡时A、B的转化率之比为a:b
C. 若a+b = c+d,往含m mol气体的平衡体系中充入n mol B,则达到平衡时气体总物质的量等于(m+n)mol。
D. 若a+b = c,对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.根据纤维在火焰上燃烧产生的气味,确定该纤维是否为蛋白质纤维
B.焰色反应实验可用细铁丝代替铂丝
C.用湿润的 pH 试纸测氯化钠溶液的 pH,对结果不影响
D.金属钠失火可用煤油来灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式错误的是( )
A.醋酸和足量的氢氧化钠溶液反应:H++OH﹣═H2O
B.溴化亚铁溶液中通入足量的氯气:2 Fe2++4 Br﹣+3 Cl2═2 Fe3++2 Br2+6 Cl﹣
C.用小苏打治疗胃酸过多:HCO ![]() +H+═CO2↑+H2O
+H+═CO2↑+H2O
D.碳酸氢铵稀溶液中加入过量的石灰水:Ca2++HCO ![]() +2 OH﹣+NH
+2 OH﹣+NH ![]() ═CaCO3↓+NH3?H2O+H2O
═CaCO3↓+NH3?H2O+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化硫酰(SO2Cl2)主要用作氯化剂。它是一种无色液体,熔点—54.1℃,沸点69.1℃,遇水生成硫酸和氯化氢。氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:SO2(g)+Cl2(g)![]() SO2Cl2(l) △H= -97.3kJ/mol
SO2Cl2(l) △H= -97.3kJ/mol
(1)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是______(填写序号)。
A.缩小容器体积 B.使用催化剂 C.增加SO2浓度 D.升高温度
(2)已知20℃时,AgCl的溶解度为0.00015 g,Ag2SO4的溶解度为0.796 g。则SO2Cl2溶于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是____________。
(3)300℃时,体积为1L的密闭容器中充入a mol SO2Cl2,达到平衡时容器中含SO2 b mol,则300℃时合成SO2Cl2反应的平衡常数为_____________。
(4)将(3)所得的平衡混合气溶于足量的BaCl2溶液中,计算最终生成沉淀的质量(写出计算过程)________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
A.Na2CO3 NaCl NaOHB.NaCl NaOH Na2CO3
C.NaOH NaCl Na2CO3D.NaCl Na2CO3 NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当我们外出旅游的时候,在车站会看到这样的告示:严禁携带易燃、易爆、剧毒品、易腐蚀品等上车。现有:①汽油 ②酒精 ③鞭炮 ④浓硫酸 其中旅客不可带上车的是( )
A. 只有①③B. 只有②④C. 只有①②③D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com