
水的电离过程为H2O H++OH-,在25℃、35℃时其离子积分别为
H++OH-,在25℃、35℃时其离子积分别为
K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
A.水的电离过程是吸热过程
B.c(H+)随着温度的降低而升高
C.在35℃时,纯水中c(H+)>c(OH-)
D.水的电离度α(25℃)>α(35℃)
科目:高中化学 来源: 题型:
下列卤代烃在KOH醇溶液中加热不反应的是( )
 ③(CH3)3C—CH2Cl ④CHCl2—CHBr2
③(CH3)3C—CH2Cl ④CHCl2—CHBr2
⑤ ⑥CH3Cl
⑥CH3Cl
A.①③⑥ B.②③⑤ C.全部 D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关试剂的保存方法,错误的是
A.漂白粉密封保存于阴凉干燥的地方 B.少量的金属钠保存在煤油中
C.盛装NaOH溶液的试剂瓶用橡皮塞 D.新制的氯水保存在无色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
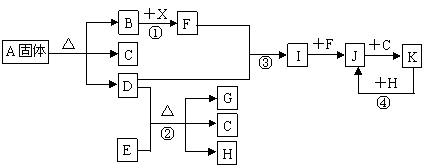 下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
请按要求填空:
(1)A物质的化学式是 ▲ ;
(2)反应③的化学方程式是 ▲ ;
反应④的离子方程式是 ▲ ;
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是 ▲ ;
(4)检验溶液A中阳离子的方法是 ▲
;
(5)反应②中氧化剂是 ▲ ;
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式(Q1、Q2均为正值):
C(s)+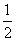 O2(g) ===CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) ===CO2(g) ΔH=-Q2 kJ·mol-1,
O2(g) ===CO(g) ΔH=-Q1 kJ·mol-1,C(s)+O2(g) ===CO2(g) ΔH=-Q2 kJ·mol-1,
有关上述反应的叙述错误的是
A.Q1<Q2 B.生成物总能量均高于反应物总能量
C.由1 mol C反应生成1 mol CO气体时放出Q1 kJ的热量
D.1 mol CO2气体具有的能量大于1 mol干冰具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出]。乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,t3~t4阶段为使用催化剂。下列说法中正确的是
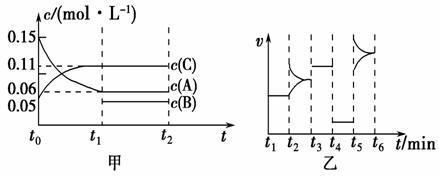
A.若t1=15 s,用A的浓度变化表示t0~t1阶段的平均反应速率为0.004 mol·L-1·s-1
B.该容器的容积为2 L,B的起始物质的量为0.02 mol
C.t4~t5阶段改变的条件一定为减小压强
D.t5~t6阶段,容器内A的物质的量减少了0.06 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式:3A(g) B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.反应NH3(g) + HCl (g)== NH4Cl(s)在室温下可自发进行,则该反应的△H <0
C.用电解水的方法制取大量氢气可以缓解能源不足的问题
D.升高温度活化能降低
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C均为气体,A 与B反应生成C。某温度下,向容积固定的密闭容器中充入一定浓度的A与B,A的起始浓度为1mol/L、B的起始浓度x mol/L。反应过程中密闭容器内的压强始终不变,反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。
(1)x = ________
(2)2min内反应的平均速率为:v (B) = _________________
(3)用不同物质表示该反应速率,其数值之间的关系是:v (B) =__________v (C)
(4)该反应的化学方程式为:____________________________________________________
(5)该反应平衡常数K的表达式是:K= ,该温度下,反应的平衡常数是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
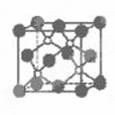
磷化硼是一种超硬耐磨涂层材料。右图为其晶体结构中
最小的重复结构单元,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( )
A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4个共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com