
| A. | N2为还原产物 | |
| B. | 当x=2时,每生成1 mol N2,转移电子数为4 mol | |
| C. | 等物质的量N2和CO2中,共价键的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
分析 NOx+CO→N2+CO2反应中,C元素的化合价升高,则N元素的化合价降低,x=2时,N元素由NO2中+4价降低为N2中0价,以此来解答.
解答 解:A.该反应中氮化合价由+2x价降低到0价,被还原,氮气为还原产物,故A正确;
B.x=2时,N元素由NO2中+4价降低为N2中0价,转移电子物质的量为N原子的4倍,每生成1mol N2,转移电子数为1mol×2×4=8mol,故B错误;
C.N2分子中含有N≡N三键,1molN2含有3mol共价键,CO2分子中含有2个C=O双键,1molCO2含有4mol共价键,故等物质的量N2和CO2中,共用电子对的个数比为3:4,故C正确;
D.令NOx中N元素的化合价为a,由氧化剂与还原剂的物质的量之比为1:1,则1×(a-0)=1×(4-2),解得a=2,故D正确.
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意利用化合价计算转移电子,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所用氢氧化钠已经潮解 | |
| B. | 向容量瓶中加水未到刻度线 | |
| C. | 有少量的氢氧化钠残留在烧杯中 | |
| D. | 用带游码的托盘天平称2.4g氢氧化钠时误用了“左码右物”的操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
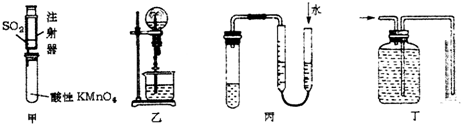
| A. | 可用甲装置来探究SO2的漂白性 | |
| B. | 可用乙装置验证HCl气体极易溶于水 | |
| C. | 用图示的方法可以检查丙装置的气密性 | |
| D. | 可用丁装置测量铜与稀硝酸反应生成气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
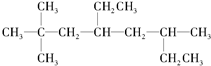 烃A的一氯代物具有不同沸点的产物有10种.
烃A的一氯代物具有不同沸点的产物有10种.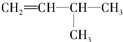 的系统名称是3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷.
的系统名称是3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷.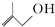 的分子式为C4H8O;
的分子式为C4H8O;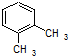 名称为:1,2-二甲基苯(或邻二甲苯).
名称为:1,2-二甲基苯(或邻二甲苯).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com