
����Ŀ���ζ�ʵ���ǻ�ѧѧ������Ҫ�Ķ���ʵ�飮 ��֪ijNaOH�����к���NaCl���ʣ�Ϊ�ⶨ������NaOH��������������������ʵ�飺
�ٳ���1.0g��Ʒ����ˮ�����250mL��Һ��
��ȷ��ȡ25.00mL������Һ����ƿ�У�
�۵μӼ��η�̪��Һ��
����0.1000mol/L�ı�����ζ����Σ�ÿ����������������¼�����
�ζ���� | ����Һ�����mL�� | �����ı�����������mL�� | |
�ζ�ǰ | �ζ��� | ||
�� | 25.00 | 0.50 | 20.60 |
�� | 25.00 | 6.00 | 26.00 |
�� | 25.00 | 1.10 | 21.00 |
��ش��������⣺
��1���ζ��յ�ʱ�������� ��
��2�������Ƶ�250mL��ƷҺ��NaOH�����ʵ���Ũ���� molL��1��������NaOH����������Ϊ ��
��3������������������ⶨ���ƫ�ߵ��� �� a���ζ�ǰ������ˮ��ϴ��ƿ
b����ҡ����ƿʱ������ƿ����Һ����
c���ζ�ǰ�����ݣ��ζ���������ʧ
d����ʽ�ζ��ܵ����յ�ԣ����Ӷ���
e����ʽ�ζ���������ˮϴ��δ�ñ�Һ��ϴ��
���𰸡�
��1��dz��ɫ��Ϊ��ɫ,30S����ɫ
��2��0.08��80%
��3��ce
���������⣺��1���μӼ��η�̪��NaOH��Һ�Ժ�ɫ�����ζ����յ�ʱ����Һ�����ԣ���Һ��Ϊ��ɫ�����Դ��ǣ�dz��ɫ��Ϊ��ɫ��30S����ɫ����2����0.10mol/L�ı�����ζ����Σ����������ƽ�����Ϊ ![]() mL=20.00mL��
mL=20.00mL��
HCl�� | NaOH |
1 | 1 |
0.10mol/L��20mL | n��NaOH�� |
����֮��n��NaOH��=0.002mol���������ʵ���Ũ��Ϊ�� ![]() =0.08mol/L��
=0.08mol/L��
���ռ���Ʒ�Ĵ���Ϊ ![]() =80%�����Դ��ǣ�0.08��80%����3��a���ζ�ǰ������ˮ��ϴ��ƿ�������Ӱ�죻
=80%�����Դ��ǣ�0.08��80%����3��a���ζ�ǰ������ˮ��ϴ��ƿ�������Ӱ�죻
b��������ƿʱ������ƿ����Һ���������ƫ�ͣ�
c���ζ�ǰ���ζ��ܼ��첿�������ݣ��ζ���������ʧ��NaOH��Һ���ƫ�࣬����c�����⣩= ![]() ������c�����⣩ƫ�ߣ�
������c�����⣩ƫ�ߣ�
d����ʽ�ζ��ܵ����յ�ԣ����Ӷ������������ƫС�����ƫ�ͣ�
e����ʽ�ζ���������ˮϴ��δ�ñ�Һ��ϴ����Ҫ��������ᣬ���ƫ�ߣ�
��ѡce��
�����㾫������������к͵ζ��ǽ����ĸ�������Ҫ֪���к͵ζ�ʵ��ʱ��������ˮϴ���ĵζ������ñ�Һ��ϴ����װ��Һ�����ô���Һ��ϴ������ȡҺ�壻�ζ��ܶ���ʱ�ȵ�һ�����Ӻ��ٶ������۲���ƿ����Һ��ɫ�ĸı�ʱ���ȵȰ������ɫ�����Ϊ�ζ��յ㣮


 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ�ý���ʵ�飬���ش��������⣺ 
��1���ж�װ�õ����ƣ�A��Ϊ ��
��2��п�缫��ӦʽΪ �� ʯī��C1Ϊ�����缫��ӦʽΪ �� ʯī��C2����������ʵ������Ϊ ��
��3����C2������2.24L���壨��״̬��ʱ��п������������g��CuSO4��Һ������������g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧѡ��3�����ʽṹ�����ʡ�
�������ʯ�е�һ�֣�����Ҫ�ɷ�Ϊ��������-NaAI(Si2O6)��������Cr��Ni��Mn��Mg��Fe��Ԫ�ء��ش��������⣺
(l)��̬Crԭ�ӵĵ����Ų�ʽΪ____��Feλ��Ԫ�����ڱ���___ ����
(2)�������Ҫ�ɷֹ���ê�Ʊ�ʾΪ������Ļ�ѧʽΪ____����������Ԫ�ص�һ��������С�����˳����____��
(3)�ƺ������ǵ�������Ԫ�أ���ԭ�ӵ�������������ͬ��Ϊʲô�����۷е�Զ���ڸƣ�____��
(4)�ڹ������д���![]() �ṹ��Ԫ������Siԭ�ӵ��ӻ��������Ϊ____�������������n��ʾ��
�ṹ��Ԫ������Siԭ�ӵ��ӻ��������Ϊ____�������������n��ʾ��![]() �ֱ���3��������������3��
�ֱ���3��������������3��![]() �γɲ�״�ṹʱ����ͼ��ʾ��������Si��Oԭ�ӵ���Ŀ֮��Ϊ____��
�γɲ�״�ṹʱ����ͼ��ʾ��������Si��Oԭ�ӵ���Ŀ֮��Ϊ____��
��������һ���Si��Al�滻���仯ѧʽΪ____��
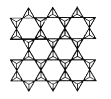
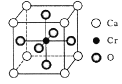
(5) Cr��Ca�����γ��־���������Եĸ�������������ṹ��ͼ��ʾ���þ���Ļ�ѧʽΪ____����Ca��O�ĺ˼����Ϊx nm����þ�����ܶ�Ϊ___ g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863 �ƻ���
(1)���������н�ǿ��ѡ���ԡ���֪:
��ӦI:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
4NO(g)+6H2O(g) ��H1=-905kJ��mol-1
��ӦII:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
2N2(g)+6H2O(g) ��H2=-1266.6kJ��mol-1
д��NO �ֽ�����N2��O2���Ȼ�ѧ����ʽ______________________________________��
(2)N2OҲ�ɷֽ�����N2��O2�����ĸ������ܱ������а����±���Ӧ���������壬����2N2O(g)![]() 2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
2N2(g)+O2(g)������I��II��III��N2Oƽ��ת��������ͼ��ʾ��
���� | �ݻ�/L | ��ʼ���ʵ���/mol | ||
N2O | N2 | O2 | ||
I | V1 | 0.1 | 0 | 0 |
II | 1.0 | 0.1 | 0 | 0 |
III | V2 | 0.1 | 0 | 0 |
IV | 1.0 | 0.06 | 0.06 | 0.04 |
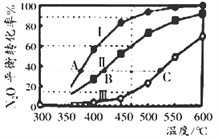
�ٸ÷�Ӧ�ġ�H_________0(�>������=������<��);
��ͼ��A��B��C ���㴦�����ڵ���ѹǿ���ɴ�С��˳����_____________________��
������IV��470����з�Ӧʱ����ʼ����:v(N2O)��____v (N2O)��(�>������=������<��)��
(3)��������ʱ�ᷢ����������������ӦI��II��Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���20L�ܱ������г�lmolNH3��2molO2�����һ��ʱ�����й����ʵ�����ϵ��ͼ:
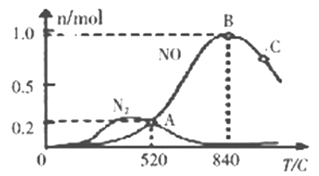
�ٸô����ڵ���ʱѡ��Ӧ________(�I����II��)��
��C���B����������NO�����ʵ����ٵ�ԭ�������_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ����У����������ǣ� ��
A.NaOH��ǿ�
B.CO2�������
C.H2SO4�����ᣩ
D.���ᣨ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�����ṹ��ʽ��ͼ�����ڸ��л��������������ȷ���ǣ� ��
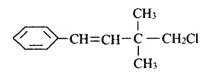
A. ��ʹ����KMnO4��Һ����ˮ��ɫ��ԭ����ͬ
B. 1 mol���л�������H2������Ӧ������H2���ʵ���Ϊ4mol
C. һ�������£��ܷ����Ӿ۷�Ӧ
D. ���л��ﱽ���ϵ�һ��H��ȡ������3��ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ��˵����ȷ���ǣ������� 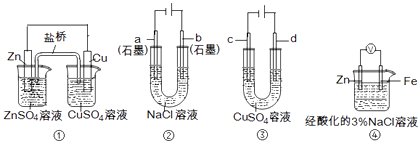
A.װ�â��У������е�K+����ZnSO4��Һ
B.װ�âڹ���һ��ʱ���a��������Һ��pH����
C.��װ�â۾���ͭʱ��c��Ϊ��ͭ
D.װ�â��е�����Zn����Fe��װ������Fe2+����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ��ܱ������У�����4mol����A��2mol����B������Ӧ��3A��g��+2B��g��4C������+2D����������Ӧһ��ʱ���ﵽƽ�⣬�������1.6mol C����Ӧǰ����ϵѹǿ֮��Ϊ5��4��������˵����ȷ���ǣ�������
A.����A��ƽ��ת���ʴ�������B��ƽ��ת����
B.����D�ľۼ�״̬һ��������
C.ƽ��������¶ȣ���ƽ�������ƶ���������Ӧ�ġ�H��0
D.ƽ�������С����ϵ��ѹǿ����ƽ�������ƶ�����ѧƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������ܱ������з�����ѧ��Ӧ��Fe2O3(s) +2NH3(g)![]() 2Fe(s)+N2(g)+3H2O(g) ��H��ʵ���û�ѧƽ��ʱ���йر仯������ͼ��ʾ����֪��ƽ�ⳣ������ƽ���ѹ����ƽ��Ũ�ȼ��㣬�����ѹ=������ѹ�����ʵ�������������˵������ȷ����
2Fe(s)+N2(g)+3H2O(g) ��H��ʵ���û�ѧƽ��ʱ���йر仯������ͼ��ʾ����֪��ƽ�ⳣ������ƽ���ѹ����ƽ��Ũ�ȼ��㣬�����ѹ=������ѹ�����ʵ�������������˵������ȷ����
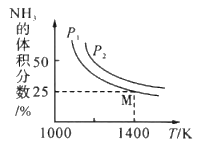
A. �÷�Ӧ�ġ�H>0
B. ����ѹǿP2 >P1
C. ƽ����ټ���Fe2O3����NH3ת��������
D. M���ƽ�ⳣ��Kp=![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com