
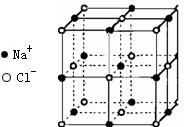
 (4)晶体中,Fe离子间最近距离为 cm
(4)晶体中,Fe离子间最近距离为 cm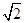 ×(4.28×10―10)/2 m=3.03×10―10m==3.03×10―8cm
×(4.28×10―10)/2 m=3.03×10―10m==3.03×10―8cm

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.仅有① | B.仅有①④⑤ | C.仅有②③④ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

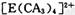 配离子,其中存在的化学键类型有 ______ (填序号);
配离子,其中存在的化学键类型有 ______ (填序号);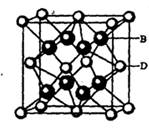
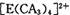 具有对称的空间构型,且当
具有对称的空间构型,且当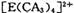 中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则
中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则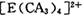 的空间构型为 ____________ (填序号);
的空间构型为 ____________ (填序号);查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.由于NaCl 晶体和CsCl晶体中正负离子半径比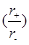 不相等,所以两晶体中离子的配位数不相等 不相等,所以两晶体中离子的配位数不相等 |
| B.CaF2晶体中,Ca2+配位数为8,F-配位数为4不相等,主要是由于F-、Ca2+电荷(绝对值)不相同 |
| C.MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大 |
| D.MCO3中M2+半径越大,MCO3热分解温度越低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 晶 ④水银 ⑤氧化铝 ⑥P4 ⑦苯
晶 ④水银 ⑤氧化铝 ⑥P4 ⑦苯 | A.分子晶体 | B.原子晶体 | C.离子晶体 | D.金属晶体E.混合晶体 |
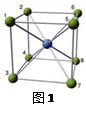
 宏观外形为 。
宏观外形为 。
元素代 号 号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子晶体中只存在非极性共价键 |
| B.稀有气体形成的晶体属于分子晶体 |
| C.干冰升华时,分子内共价键会发生断裂 |
| D.分子晶体的熔点普遍都很高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
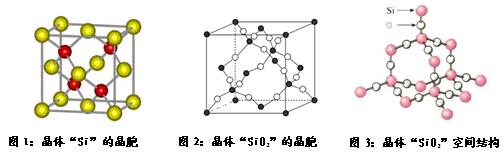
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 晶体一定是分子晶体 ⑥.元素周期表从ⅢB族到ⅡB族8个纵行的元素都是金属元素 ⑦.在 SiO2和干冰晶体中,都存在单个分子
晶体一定是分子晶体 ⑥.元素周期表从ⅢB族到ⅡB族8个纵行的元素都是金属元素 ⑦.在 SiO2和干冰晶体中,都存在单个分子| A.①②⑤ | B.②④⑤ | C.②⑤⑧ | D.①④⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是 ( )
属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是 ( )| A.K3C60中既有离子键,又有极性键 |
| B.1 molK3C60中含有的离子数目为63×6.02×1023 |
| C.该晶体在熔融状态下能导电 |
| D.该物质的化学式可写为KC20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com