
新型高效 的甲烷燃料电池采用铂为
的甲烷燃料电池采用铂为 电极材料,两电极上分别通入CH4和O2 ,
电极材料,两电极上分别通入CH4和O2 ,
电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如
图所示。
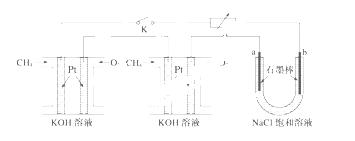
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为______ __________、____________________。
__________、____________________。
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是__________,电解氯化钠溶液的总反应方程式为__________________________________________________________;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1列式计算),最多能产生的氯气体积为________L(标准状况)。
科目:高中化学 来源: 题型:
糕点包装中常见的脱氧剂组成为还原性铁粉、氯
化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应,脱氧的同时可降低温度,延长糕点保质期
B.脱氧过程中铁做原电池正极,电极反应为:Fe—2e— = Fe2+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e— = 4OH—
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
为检验某溴代烃(R-Br)中的溴元素,有下列实验操作:
①加热煮沸 ②加入AgNO3溶液 ③取少量卤代烃 ④加入稀硝酸酸化 ⑤加入NaOH溶液 ⑥冷却,正确 操作的先后顺序是 ( )
操作的先后顺序是 ( )
A. ③①⑤⑥②④ B.③①②⑥④⑤
③①⑤⑥②④ B.③①②⑥④⑤
C.③⑤①⑥④② D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关用惰性电极电解AgNO3溶液一段时间后的说法正确的是 ( )
A.电解过程中阳极质量不断增加
B.电解过程中溶液的pH不断升高
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙
述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
A.阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.SiO2制成的纤维,由于导电能力强而被用于制造光缆
B.用一束光线通过氯化钠溶液和蛋白质溶液,能看到相同的现象
C.SO2和Cl2通入品红溶液,品红均褪色,说明两者的漂白原理相同
D.浓硝酸具有强氧化性,能使铝钝化,故常用铝罐车运输冷的浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛用在有机合成、化学分析等领域。
(1)海水提溴过程中溴元素的变化如下 :
:
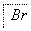
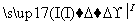
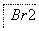
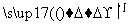
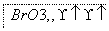
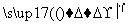
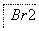
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。
ⅰ.通入氯气后,反应的离子方程式是_______________________。
ⅱ.调海水pH可提高Cl2的利用率,用平衡原理解释其原因是______。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
 Br2+
Br2+ Na2CO3===
Na2CO3=== NaBrO3+
NaBrO3+ CO2+
CO2+ ________
________
③过程Ⅲ,用硫酸酸化可得Br2和Na2SO4的混合溶液。
相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是__________是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
| 粒子 | I2 | Br2 | IO |
| 物质的量/mol | 0.5 | 1.3 |
则原溶液中NaI的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素
周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A.X的最常见气态氢化物的水溶液显酸性
B.最高价氧化物对应水化物的酸性W比Z强
C.Z的单质与氢气反应较W剧烈
D.X的原子半径小于Y
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁、戊五种短周期元素原子序数依次递增。甲最
外层电子数是次外层的两倍,丙的次外层电子数比最外层少4个,丁形成的简单阳离子是同周期元素简单
离子中半径最小的,戊是同周期主族元素中原子半径最小的。试用化 学式回答下列问题:
学式回答下列问题:
(1)乙和戊形成的化合物中各原子最外层均满足8e-结构,其化学式为 ;
(2)写出乙的最高价氧化物的水化物的浓溶液与甲单质反应的化学方程式
;
(3)戊的最高价氧化物与丁的最高价氧化物的水化物反应的离子反应方程式为
;
(4) 常温下戊单质被NaOH溶液吸收的化学方程式为 ;
(5)氢与丙形成原子个数比为1:1的液体,该物质中存在的作用力有( )
①极性键 ②非极性键 ③离子键 ④氢键 ⑤范德华力
④氢键 ⑤范德华力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com