
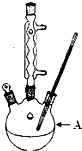
 苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)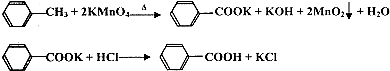
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
分析 (1)根据常用仪器的名称来解答;本实验控制反应温度约在100℃,可以采用水浴加热;
(2)实验使用了KMnO4做氧化剂,白色粗产品中除了KCl外,还有MnCl2;
(3)苯甲酸在25℃和95℃时溶解度分别为0.3g和6.9g,操作②是要获得苯甲酸溶液,要尽量减小苯甲酸的损失,从混合液中得到沉淀一般采用过滤、干燥;
(4)步骤③中涉及一定物质的量浓度溶液的配制;
(5)第三次数据与其它数据差别较大舍去,平均消耗体积为24.00mL,求出KOH的物质的量,根据反应方程式中物质之间量的关系求出苯甲酸的物质的量,再求转化率和质量分数;
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视,两次度数距离偏小,测定结果也偏小.
解答 解:(1)由实验装置图可知A为三颈烧瓶;本实验控制反应温度约在100℃,可以采用水浴加热,而且要沸水加热,
故答案为:三颈烧瓶;沸水浴加热;
(2)实验使用了KMnO4做氧化剂,KMnO4中性条件下还原产物为MnO2,同时还生成KOH,再加浓盐酸,除了生成苯甲酸,还有KCl和MnCl2生成,所以可能的无机杂质为为KCl和MnCl2;
故答案为:MnCl2;
(3)苯甲酸在25℃和95℃时溶解度分别为0.3g和6.9g,操作②是要获得苯甲酸溶液,要尽量减小苯甲酸的损失,所以过滤时要趁热,防止苯甲酸结晶析出,减少其损失,将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,生成的苯甲酸溶解度较小,以晶体的形式析出,从混合液中得到沉淀一般采用过滤、干燥;
故答案为:防止苯甲酸结晶析出,减少其损失;过滤、干燥;
(4)步骤③中涉及配制100mL苯甲酸溶液,需要定量仪器100mL容量瓶,故答案为:100mL容量瓶;
(5)第三次数据与其它数据差别较大舍去,平均消耗体积为$\frac{24.00+24.10+23.90}{3}$=24.00mL,则消耗的KOH的物质的量为0.1000mol/L×0.02400L=0.002400mol,苯甲酸( )中含有一个羧基,与氢氧化钾等物质的量恰好反应,则苯甲酸的物质的量为0.002400mol;晶体中苯甲酸的总物质的量为0.002400mol×$\frac{100ml}{25ml}$=0.009600mol,则样品中苯甲酸纯度为$\frac{0.009600mol×122g/mol}{1.220g}$×100%=96.00%;
)中含有一个羧基,与氢氧化钾等物质的量恰好反应,则苯甲酸的物质的量为0.002400mol;晶体中苯甲酸的总物质的量为0.002400mol×$\frac{100ml}{25ml}$=0.009600mol,则样品中苯甲酸纯度为$\frac{0.009600mol×122g/mol}{1.220g}$×100%=96.00%;
故答案为:96.00%;
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视,两次度数距离偏小,即氢氧化钾的体积偏小,则消耗的氢氧化钾的物质的量偏小,求出的苯甲酸的物质的量偏小,所以苯甲酸的质量和质量分数也偏小,故答案为:偏小.
点评 本题考查了苯甲酸的制备实验方案设计,为高考常见题型,侧重于制备实验操作、物质的分离提纯、数据的处理和计算、滴定原理的应用等知识点的考查,清楚制备的原理是解答的关键,题目难度中等.


科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:选择题
下列说法正确的是
A.标准状况下,22.4L水的物质的量为1摩尔
B.常温常压下,32g O3气体物质的量为1摩尔
C.标准状况下,a L的氧气和氮气的混合物含有的分子数约为a/22.4×6.02×1023
D.2.24L CO2中含有的原子数为0.3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 已知如表数据:
已知如表数据:| 物 质 | 2,4,6 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 乙 醇 | -114 | 78 | 0.789 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
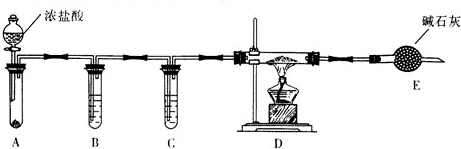
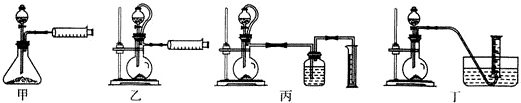
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
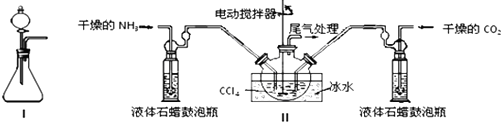
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解. | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置. | 溶液变浑浊,则证明固体中含有(NH4)2CO3. |
| 步骤3:取步骤2的上层清液于试管中加入少量的Ba(OH)2溶液. | 溶液不变浑浊,则证明固体中不含有NH4HCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.在实验室我们可以用如图所示的装置来制取乙酸乙酯.回答下列问题: CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
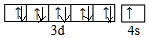 .
.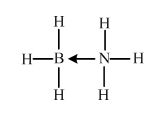 (必须标明配位键).
(必须标明配位键).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验 序号 | 浓度 mol•L-1 温度(℃)时间( min) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(g)+O2(g)=SO2(g)+Q3 Q3>297.16 kJ | |
| B. | 单斜硫和正交硫互为同分异构体 | |
| C. | 常温下单斜硫比正交硫稳定 | |
| D. | 单斜硫转化为正交硫的反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com