
 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18 列中的第7列元素.D的原子序数比E小5,D跟B可形成离化合物其晶胞结构如图.
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18 列中的第7列元素.D的原子序数比E小5,D跟B可形成离化合物其晶胞结构如图.分析 A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等,则A为H元素;E是周期表中1-18 列中的第7列元素,可判断E是第4周期VIIB族的Mn元素,原子序数为25,D的原子序数比E小5,则D的原子序数为20,故D为Ca元素;D跟B可形成离化合物,其晶胞中D与B的离子个数比值为:(8×$\frac{1}{8}$+6×$\frac{1}{2}$):8=1:2,则B的化合价为-1价,应为第ⅦA族元素,B和C属同一主族,B的原子序数较小,则B为F,C为Cl,D跟B形成的离子化合物为CaF2,计算晶胞质量,根据V=$\frac{m}{ρ}$计算晶胞体积.
解答 解:A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.其中A原子所处的周期数、族序数都与其原子序数相等,则A为H元素;E是周期表中1-18 列中的第7列元素,可判断E是第4周期VIIB族的Mn元素,原子序数为25,D的原子序数比E小5,则D的原子序数为20,故D为Ca元素;D跟B可形成离化合物,其晶胞中D与B的离子个数比值为:(8×$\frac{1}{8}$+6×$\frac{1}{2}$):8=1:2,则B的化合价为-1价,应为第ⅦA族元素,B和C属同一主族,B的原子序数较小,则B为F,C为Cl.
(1)A为H元素,名称为氢,故答案为:氢;
(2)B为F元素,C为Cl元素,故答案为:F;Cl;
(3)E为Mn元素,位于周期表第四周期第七列,则应位于VIIB族,原子的核外电子的排布式为1s22s22p63s23p63d54s2,+2价离子的电子排布式为1s22s22p63s23p63d5,
故答案为:四;VIIB; 锰; 1s22s22p63s23p63d5;
(4)从图中可以看出,晶胞中含有Ca的离子个数为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,含有F的离子个数为8,二者比值为1:2,则化学式为CaF2,晶胞V=$\frac{\frac{78g/mol}{6.02×1{0}^{23}mo{l}^{-1}}×4}{ag.c{m}^{-3}}$=$\frac{4×78g/mol}{ag.c{m}^{-3}×6.02×1{0}^{23}mo{l}^{-1}}$,
故答案为:CaF2;$\frac{4×78g/mol}{ag.c{m}^{-3}×6.02×1{0}^{23}mo{l}^{-1}}$.
点评 本题是对物质结构的考查,涉及核外电子排布、晶胞计算等,推断元素是解题关键,注意利用均摊法进行晶胞有关计算,难度中等.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
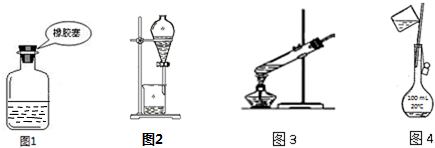
| A. | 图1装置:存放NaOH溶液 | |
| B. | 图2装置:分离乙酸乙酯和水 | |
| C. | 图3装置:葡萄糖的银镜反应 | |
| D. | 图4装置:配制 100 mL 1 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至多有26个原子处于同一平面上 | |
| C. | 该烃能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 | |
| D. | 该烃属于苯的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 .元素①的最高价氧化物的电子式:
.元素①的最高价氧化物的电子式: ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁在空气中和纯净氧气中的燃烧产物只有MgO | |
| B. | 硫在空气中的燃烧产物是SO2,在纯净氧气中的燃烧产物是SO3 | |
| C. | 钠在敞口容器中长期放置和在空气中燃烧的产物都是Na2O2 | |
| D. | 浓H2SO4和浓盐酸敞口放置在空气中,其溶质的质量分数都将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 气体 | O2 | CO2 | HCl |
| 试剂 |
| 装置 | 该装置中反应的离子方程式 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X和W组成的化合物属于分子晶体 | |
| B. | Y的气态氢化物比Z的气态氢化物稳定 | |
| C. | X的单质既能与NaOH溶液反应,又能与氢氟酸反应 | |
| D. | 向KI-淀粉溶液中通入某气体后变蓝,则该气体一定是Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com