
为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下图。下列说法正确的是

溶液X为稀硫酸,气体Y为氨气
由溶液F获得溶质F固体的过程中,须控制条件防止其氧化和分解
使用足量稀硫酸时,试剂Z选用H2O2或适量HNO3均获得胆矾晶体
D、操作①为过滤,操作②为蒸发结晶、洗涤、干燥
科目:高中化学 来源:2015-2016学年浙江省温州市十校联合高二下期中化学试卷(解析版) 题型:选择题
某同学设计了由乙醇合成乙二醇的路线如下。下列说法正确的是( )
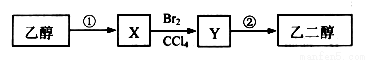
A. X可以发生加成反应
B. 等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同
C. 步骤②需要在氢氧化钠醇溶液中反应
D. 步骤①的反应类型是水解反应
查看答案和解析>>
科目:高中化学 来源:2016届河南省原推荐高三四月高考仿真模拟理综化学试卷(解析版) 题型:简答题
【化学——选修3:物质结构与性质】
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____________,1mol(C2H5O)3P=O分子中含有的σ键的数目为__________________。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
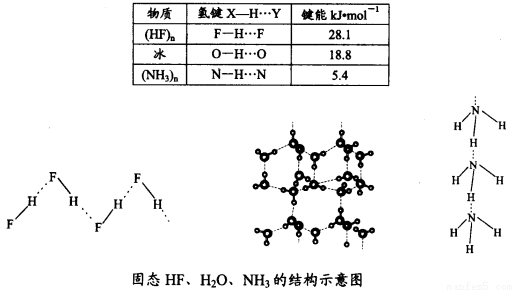
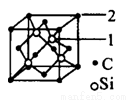
解释H2O、HF、NH3沸点依次降低的原因___________________。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________个,与碳原子等距离最近的碳原子有__________个。已知碳化硅晶胞边长为apm,则晶胞图中1号硅原子和2号碳原子之间的距离为________pm,碳化硅的密度为__________g/cm3。
查看答案和解析>>
科目:高中化学 来源:2016届广东省佛山市高三4月二模理综化学试卷(解析版) 题型:填空题
己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:3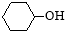 +8HNO3 —→ 3
+8HNO3 —→ 3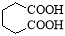 +8NO↑+7H2O
+8NO↑+7H2O

实验步骤如下:
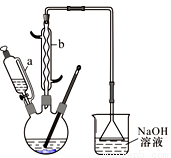
Ⅰ.在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31 g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60 ℃~65 ℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80 ℃~90 ℃水浴加热约10 min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)装置b的名称为 ,使用时要从 (填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是
(2)本实验所用50%的硝酸的物质的量浓度为 ;实验中,氮氧化物废
气(主要成分为N02和NO)可以用NaOH溶液来吸收,其主要反应为:
2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20
其中NaOH溶液可以用Na2C03溶液来替代,请模仿上述反应,写出Na2C03溶液吸收的两个方程式:
;
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(4)为了除去可能的杂质和减少产品损失,可分别用 和 洗涤晶体。
查看答案和解析>>
科目:高中化学 来源:2016届广东省佛山市高三4月二模理综化学试卷(解析版) 题型:选择题
伞形酮可由雷琐苯乙酮和苹果酸在一定条件下反应制得,下列说法错误的是
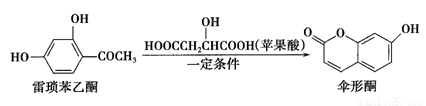
A.雷琐苯乙酮有两种含氧官能团
B.1mol伞形酮与足量NaOH溶液反应,最多可消耗2molNaOH
C.伞形酮难溶于水
D.雷琐苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高考模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A、蒸馏实验开始时应先加热后通冷凝水
B、不能用湿润的pH试纸测定溶液的pH,否则必然会使实验结果产生误差
C、提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)应过量
D、在中和热测定实验中,为准确测得反应前后的温差,应将已分别测得温度的氢氧化钠溶液与盐酸在量热剂中快速混合,并不断轻轻搅拌,测量混合液的最高温度
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三下学期八校联考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.0.02 mol•L—1醋酸与0.02 mol•L—1NaOH等体积混合后的溶液中加少量的CH3COONa固体则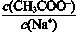 增大
增大
B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0
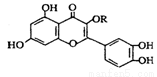
C.lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol
D.红外光谱分析不能区分乙醇和乙醚
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期中化学试卷(解析版) 题型:选择题
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,不能说明反应A(s)+2B(g) C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
已知298 K时,合成氨反应:N2(g)+3H2(g) 2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在体积为2L的密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ;原因是
2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在体积为2L的密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ;原因是
如果反应5分钟达到平衡时气体总物质的量为2.5mol,则这段时间内氢气的反应速率为 ,达平衡时氮气的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com