
【题目】把4molA和2.5molB混合于2L密闭容器中,发生反应:3A(g)+2B(s)![]() xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol·L-1·min-1,错误的是
xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol·L-1·min-1,错误的是
A. A的平均反应速率为0.15mol·L-1·min-1 B. 平衡时,C的浓度为0.25 mol·L-1
C. B的平均反应速率为0.1mol·L-1·min-1 D. 平衡时,容器内压强为原来的0.875倍
【答案】C
【解析】5min后反应达到平衡,容器内压强变小,应有x+1<3,x<2,x=1,D的平均反应速率为0.1mol/(L·min),则生成n(D)=2L×5min×0.05mol/(L·min)=0.5mol,则:
3A(g)+2B(s)![]() C(g)+D(g)
C(g)+D(g)
n起始 4mol 0 0
n转化 1.5mol 0.5mol 0.5mol
n平衡 2.5mol 0.5mol 0.5mol
A、A的平均反应速率为3×0.05mol·L-1·min-1=0.15mol·L-1·min-1,故A正确;B、平衡时,C的浓度为0.5mol/2L=0.25mol·L-1,故B正确;C、B为固体,不能用单位时间内浓度变化量表示反应速率,故C错误;D、平衡时,容器内压强为原来的(2.5mol+0.5mol+0.5mol)/4mol=0.875,故D正确。故选B。


科目:高中化学 来源: 题型:
【题目】下列关于铝及其化合物的叙述正确的是( )
A.铝在常温下不会被氧气氧化B.氧化铝可用于冶炼金属铝
C.氢氧化铝不能与NaOH溶液反应D.明矾可用于饮用水消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2L的密闭容器中,A、B、C三种气态物质的物质的重随时间变化曲线如图所示。请回答以下问题:
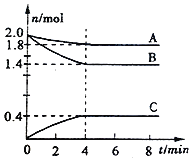
(1)该反应的化学方程式是___________。
(2)反应从开始到平衡时,气体C的平均反应速率是_______ 。
(3)反应达平衡,反应物B的转化率是___;体系的压强是开始时的______倍。
(4)其他条件不变,升高温度,逆反应速率将________(填“加快”、“减慢”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了x g,则( )
A. 电解液质量增加x g B. 阴极质量增加x g
C. 阴极质量增加a g,a>x D. 阴极质量增加b g,b<x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色溶液,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下:

第③个实验中,生成白色沉淀的量与加入![]() 的量有如下图所示的相互关系。据此可知:
的量有如下图所示的相互关系。据此可知:

(1)在原溶液中一定存在的离子有______;一定不存在的离子有______;不能确定是否存在的离子有______。
(2)写出第③个实验中发生反应的离子方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,将图中的字母代号填入下表。

溶液 | 加入的物质 | 字母代号 |
①饱和石灰水 | 通过量CO2 | ________ |
②AlCl3溶液 | 通过量NH3 | ________ |
③MgCl2、AlCl3混合溶液 | 逐滴加NaOH溶液至过量 | ________ |
④AlCl3溶液 | 逐滴加NaOH溶液至过量 | ________ |
⑤含少量HCl的AlCl3溶液 | 逐滴加NaOH溶液至过量 | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示【已知:P[c(A-)/c(HA)]=-1g[c(A-)/c(HA)]】。下列叙述不正确的是
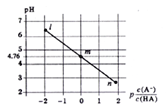
A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液过程中,c(A-)/[c(HA)×c(OH-)]保持不变
C. m点所示溶液中:c(H+)=c(HA)+c(OH-)-c(Na+)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的系统命名中,正确的是( )
A. ![]() 2,4﹣二甲基己烷
2,4﹣二甲基己烷
B. ![]() 2﹣甲基﹣4﹣戊炔
2﹣甲基﹣4﹣戊炔
C. ![]() 2,3-二甲基-2,4-戊二烯
2,3-二甲基-2,4-戊二烯
D. 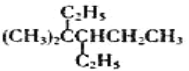 4,4—二甲基—3—乙基己烷
4,4—二甲基—3—乙基己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com