
| A. | 不能形成稳定的气态氢化物 | B. | 其原子最外层有6个电子 | ||
| C. | 其最高价氧化物的水化物是强酸 | D. | X是金属元素 |
分析 第七周期稀有气体的原子序数应为118,故116号元素处于第七周期ⅥA族,最外层电子数为6,最高正化合价为+6,金属性比Po强,属于金属元素,结合氧族元素及其化合物性质递变规律推测.
解答 解:第七周期稀有气体的原子序数应为118,故116号元素处于第七周期ⅥA族,最外层电子数为6,最高正化合价为+6,金属性比Po强,属于金属元素,
A.该元素为金属元素,其氢化物中表现正化合价,不能形成稳定的气态氢化物,故A正确;
B.116号元素处于第七周期ⅥA族,最外层电子数为6,故B正确;
C.同主族元素从上到下元素的非金属性逐渐减弱,金属性逐渐增强,其最高价氧化物的水化物应呈碱性,故C错误;
D.同主族元素从上到下元素的金属性逐渐增强,第六周期元素为Po,属于金属元素,则116号元素肯定为金属元素,故D正确,
故选C.
点评 本题考查原子结构与元素性质关系,难度不大,根据原子序数确定在周期表中的物质是关键,注意掌握同主族元素性质的相似性与递变性.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 7:8 | C. | 8:7 | D. | 5:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装置 | 现象 | 结论及解释 |
 | ①A试管中黑色沉淀逐渐溶解 ②A试管上方出现红棕色气体 ③B试管中出现白色沉淀 | a.现象②说明褐色沉淀具有 还原性. b.试管B中产生白色沉淀的总反应的离子方程式为 NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
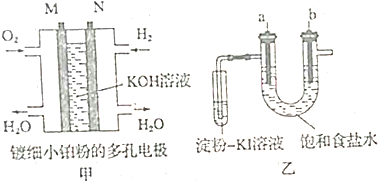
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化性:A2>B2>C2>D2 | B. | 还原性:C->A->B->D- | ||
| C. | 2A-+D2═2D-+A2的反应能进行 | D. | 2C-+B2═2B-+C2的反应不能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
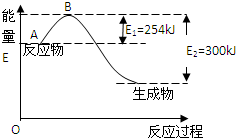 氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:
氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:| 化学键 | H-H | N≡N |
| 键能/( kJ/mol) | 435 | 943 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com