
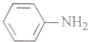
 )具有
)具有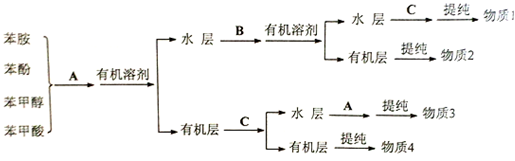
 转化为
转化为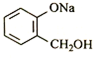 ,则应加入
,则应加入 含有氨基,具有碱性;
含有氨基,具有碱性; 含有氨基,可与盐酸反应,具有碱性,
含有氨基,可与盐酸反应,具有碱性,

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
| A、溶液中导电粒子的数目减少 | ||
B、溶液中
| ||
| C、醋酸的电离程度增大,c(OH-)亦增大 | ||
| D、再加入10 mL c(OH-)=10-3 mol?L-1的NaOH溶液,醋酸与NaOH恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
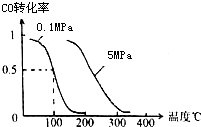 (1)在一定条件下,容积为 100L密闭容器中发生反应:
(1)在一定条件下,容积为 100L密闭容器中发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验步骤 | 简述实验操作 (不必叙述如何组装实验装置) |
| ① | 将粗盐放入烧杯中,加入适时的蒸馏水,充分搅拌,直至固体全部消失 | |
| ② | 加入NaOH溶液 | 逐滴加入氢氧化钠溶液,直至不再出现沉淀为止 |
| ③ | 加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
| ④ | 加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
| ⑤ | 过滤 | 安装好过滤器,将④烧杯中的悬浊液沿玻璃棒加入过滤器中过滤 |
| ⑥ | 滴加盐酸 | 向滤液中逐滴加入盐酸,并用pH试纸检测溶液,至溶液呈中性 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
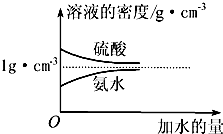 已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:| 溶质的物质的量浓度/mol?L-1 | 溶质的质量分数 | 溶液的密度/g?cm-3 | |
| 硫酸 | c1 | w1 | ρ1 |
| 氨水 | c2 | w2 | ρ2 |
| w1 |
| 2 |
| w2 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com