
A.同温同压下,  在光照和点燃条件的△H不同。 在光照和点燃条件的△H不同。 |
| B.相同条件下2mol氢原子所具有的能量小于1 mol氢分子所具有的能量 |
| C.应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
D.反应 在室温下可自发进行:则该反应的△H>0 在室温下可自发进行:则该反应的△H>0 |
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源:不详 题型:填空题
 NH2CO2NH4(s) △H1="a" kJ·mol-1
NH2CO2NH4(s) △H1="a" kJ·mol-1 CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1 CO(NH2)2(s)+H2O(g) △H3=-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g) △H3=-86.98kJ·mol-1

 (NH4)2CO3。下列物质中与尿素有类似性质的是______。
(NH4)2CO3。下列物质中与尿素有类似性质的是______。| A.NH2COONH4 | B.H2NOCCH2CH2CONH2 |
| C.HOCH2CH2OH | D.HOCH2CH2NH2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.化学能 | B.热能 | C.生物能 | D.电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a>b>c | B.a>c>b | C.c>b>a | D.b>a>c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2SO4(浓,aq)+NaOH(aq)=
H2SO4(浓,aq)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH2=m kJ·mol-1。下列说法正确的是 ( )。
Na2SO4(aq)+H2O(l) ΔH2=m kJ·mol-1。下列说法正确的是 ( )。| A.上述热化学方程式中的化学计量数表示分子个数 |
| B.ΔH1>ΔH2 |
| C.ΔH2=-57.3 kJ·mol-1 |
| D.|ΔH1|>|ΔH2| |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
| B.铝热反应会放出大量的热,因此常温下就能顺利发生 |
| C.碳酸铵[(NH4)2CO3]在室温下就能自发地分解产生氨气,碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大 |
D.对于化学反应COCl2(g) CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 CO(g)+Cl2(g) ΔH<0当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
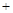 NO2(g)
NO2(g)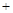 2NH3(g)
2NH3(g)  2N2(g)
2N2(g)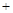 3H2O(g),
3H2O(g),
| A.上述反应的正反应为吸热反应 |
| B.催化剂①、②分别适合于250℃和450 ℃左右脱氮 |
| C.曲线①、②最高点表示此时平衡转化率最高 |
| D.相同条件下,改变压强对脱氮率没有影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应热就是反应中放出的热量 |
| B.放热反应的△H>0,吸热反应的△H<0 |
| C.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,△H为“—” |
| D.一个化学反应中,生成物的总键能大于反应物的总键能时,反应吸热,△H为“+” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com