

分析 (1)液柱高度保持不变,说明气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用;
(2)根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3;
(3)观察SO2的生成速率,发生强酸制取弱酸的反应,Ⅲ中发生S(g)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq),反应达到终点是S完全溶解,烧杯、锥形瓶需要加热时必须使用石棉网,蒸发皿、试管可直接加热;
(4)检测产品中是否存在Na2SO4,先加盐酸排除干扰,再利用氯化钡检验硫酸根离子.
解答 解:(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变;防止倒吸;NaOH;
(2)根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)观察SO2的生成速率,发生强酸制取弱酸的反应,a不生成二氧化硫,bd中物质均与二氧化硫反应,只有c中饱和NaHSO3溶液适合制取二氧化硫;Ⅲ中发生S(g)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq),反应达到终点是S完全溶解,可观察到溶液变澄清(或浑浊消失);烧杯、锥形瓶需要加热时必须使用石棉网,
故答案为:c;控制滴加硫酸的速度;溶液变澄清(或浑浊消失);ad;
(4)检测产品中是否存在Na2SO4,操作、现象和结论为取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
点评 本题考查实验方案的分析与评价,涉及气密性检验、离子检验、对操作的分析评价等,侧重实验分析能力及知识综合应用能力的考查,(2)为易错点,可以利用总反应的分析,题目难度中等.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 经常用钢丝球擦洗铝锅表面,可以防止铝锅被腐蚀 | |
| B. | 埋在地下的钢铁管道每隔一段距离就连结一定数量的铜块 | |
| C. | 供应热水的水龙头使用陶瓷制品代替钢铁制品 | |
| D. | 洗衣机的滚筒采用不锈钢材料,既耐磨又耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
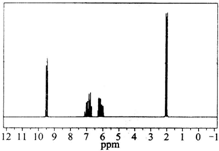 质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):
质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com