
①钠比水轻;②钠的熔点较低;③钠与水反应时要放出热量;④钠与水反应后溶液呈碱性.某学生将一小块金属钠投入滴有酚酞试液的水中,该实验能证明上述四点性质中的
A.①④ B.①②④ C.①③④ D.①②③④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.向Na2SiO3溶液中通入过量SO2:SiO32—+ SO2+ H2O=H2SiO3↓+SO32—
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.向Al2(SO4)3溶液中加入过量的NH3·H2O:Al3 ++4NH3·H2O=[Al(OH)4]—+4NH4+
D.向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
科目:高中化学 来源:2016届江西师大附中,九江一中高三上期中化学试卷(解析版) 题型:选择题
用图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法正确的是( )
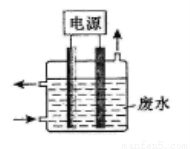
A.可以用石墨作阳极,铁作阴极
B.阳极的电极反应式为:2CN-+12OH-—10e-=N2↑+2CO32-+6H2O
C.阴极的电极反应式为: Cl-+2OH- +2e-=ClO-+H2O
D.除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O
查看答案和解析>>
科目:高中化学 来源:2016届安徽马鞍山、淮北、铜陵四校高三上第三次联考化学试卷(解析版) 题型:实验题
【化学—选修2:化学与技术】
金属钒素有“合金维生素”之称,普通钢中加入少量的钒(V)能极大地改善钢的弹性和强度。工业上回收废钒催化剂(含有V2O5、VOSO4、K2SO4、SiO2)中的钒的主要流程如下:
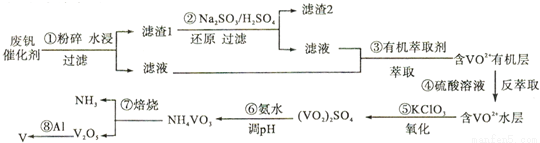
回答下列问题:
(1)滤渣l的主要成分是________________;
(2)步骤②中发生反应的离子方程式为________________;
(3)步骤③的变化过程可简化为(HA表示有机萃取剂)
VOSO4+(水层)+2HA2(有机层) VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
VOA2(有机层)+H2SO4(水层),则步骤④中可选择硫酸作萃取剂的原因是________________;萃取和反萃取在实验室里用到的玻璃仪器有______和_____;
(4)该工艺流程中,可以循环利用的物质除了氨气以外,还有____________;
(5)调节溶液pH,可将(VO2)SO4转变成NH4VO3沉淀;25℃时,当PH为1.7~1.8时,钒沉淀率为98.8%;假设其它各步反应都完全进行,已知KC1O3的还原产物是KCl,若每消耗1moiKC1O3,理论上可回收金属钒___________g(计算结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:选择题
将23 g钠和24 g镁分别放入等质量的过量的稀硫酸中,得到溶液的质量分别为a g和b g (设反应中水分不损失)则a和b的关系为
A.a=b B.a>b C.a<b D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:实验题
氮化铝(AlN)是一种新型无机非金属材料,其制取原理为:
Al2O3+3C+N2 2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
2AlN+3CO。在制取氮化铝时由于反应不完全,产品中有氧化铝和碳。
为了分析某AlN样品的组成,某实验小组进行了如下探究。
【实验1】测定样品中氮元素的质量分数。
取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).
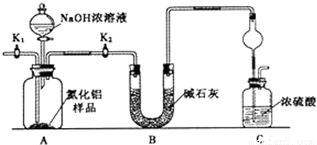
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(1)如图C装置中球形干燥管的作用是__________________________。
(2)完成以下实验步骤:组装好实验装置,首先___________,再加入实验药品.然后______,
打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,缓缓通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__________。
(3)若去掉装置B,则导致测定结果____________(填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_______________________。
【实验2】按以下步骤测定样品中铝元素的质量分数。
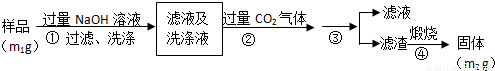
(4)步骤②生成沉淀的离子方程式为___________________。
(5)操作③需要的玻璃仪器有__________________________。
(6)A1元素的质量分数为________(用m1、m2表示)。
【实验3】测定样品中碳元素的质量分数。
称取10.00g样品置于反应器中,通往2.24LO2,在高温下充分反应后得到3.36L气体(AlN不跟O2反应),测得其密度为1.61g•L-1(体积及密度均已换算成标准状况)。
(7)计算该样品中碳元素的质量分数_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高一上期中化学试卷(解析版) 题型:填空题
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等混合而成,为检验它们做了如下实验:
(1)将固体混合物溶于水,搅拌后得无色透明溶液
(2)往此溶液中滴加硝酸钡溶液,有白色沉淀生成
(3)过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解,试判断:
固体混合物中肯定有 ,肯定没有 ,可能有 ,对可能有的物质,可采用滤液中滴加 溶液方法来检验。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:选择题
下图是425℃时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
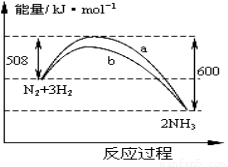
A.该反应的热化学方程式为:N2+3H2 2NH3 △H=-92kJ·mol-1
2NH3 △H=-92kJ·mol-1
B.一定条件下N2+3H2
 2NH3达到平衡时,3v正(H2) =2v逆(NH3)
2NH3达到平衡时,3v正(H2) =2v逆(NH3)
C.加入催化剂,该反应的反应热发生改变
D.温度、容器体积一定,通入1molN2和3molH2反应后放出的热量为Q1kJ,若通入2 molN2和6 molH2反应后放出的热量为Q2kJ,则有184>Q2>2Q1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com